
| A. | 固体时能导电的晶体一定为金属晶体 | |
| B. | 电负性差值小于1.7的A、B两种元素,组成的化合物也可能为离子化合物 | |
| C. | 某晶体难溶于水、熔点高、固态不导电,熔化时导电,可判断该晶体为离子晶体 | |
| D. | 由原子构成的晶体均具有熔沸点高、硬度大的特性 |
分析 A.含有自由离子或电子的物质能导电,能导电的固体不一定是金属单质;
B.一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键;
C.离子化合物的构成微粒为离子,其熔融状态下能导电,熔点高、固态不导电;
D.由原子构成的晶体可能为原子晶体、分子晶体,原子晶体具有熔沸点高、硬度大的特性,分子晶体不是.
解答 解:A.能导电的固体不一定是金属单质,如石墨,故A错误;
B.一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键,故B正确;
C.晶体难溶于水、熔点高,固态时不导电,熔化时能导电,说明熔化时有自由移动的离子,属于离子晶体,故C正确;
D.由原子间通过共价键而形成的原子晶体,具有高熔、沸点及硬度的特点,如金刚石,由原子构成的分子晶体,如稀有气体不具有熔沸点高、硬度大的特性,故D错误;
故选BC.
点评 本题考查晶体的类型及性质,注意离子化合物的构成微粒为离子,明确熔融态能导电是解答的关键,题目难度不大.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:解答题
 .
.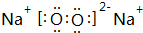 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(N2)﹕c(H2)﹕c(NH3)=1﹕3﹕2 | |
| B. | N2,H2和NH3的质量分数不再改变 | |
| C. | N2与H2的物质的量之和是NH3的物质的量的2倍 | |
| D. | 单位时间内每增加1mol N2,同时增加3mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 4 3 2 2 6 | B. | 0 2 1 0 1 2 | ||
| C. | 2 0 1 2 0 2 | D. | 2 2 2 2 1 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 银镜反应 | B. | 水解反应 | C. | 消去反应 | D. | 酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Z的分解速率和生成速率相等 | |
| B. | X、Y、Z的浓度不再变化 | |
| C. | 反应体系的总质量保持不变 | |
| D. | 单位时间内生成nmolZ,同时生成nmolX |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
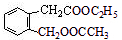 ,D的名称是乙醇.
,D的名称是乙醇.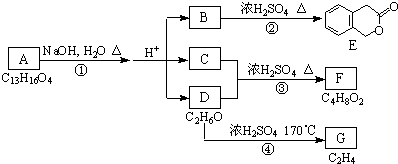
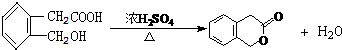 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com