
 某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:
某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:| 滴定次数 | 待测液 体积(mL) | 标准烧碱体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 4.00 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |
分析 (1)根据碱式滴定管在装液前应用所装液体进行润洗;根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断浓度的误差;
(2)根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断浓度的误差;
(3)根据滴定终点前溶液为无色,滴定结束时氢氧化钠过量,溶液显示红色判断滴定终点;
(4)根据滴定管的结构和精确度;
(5)先根据数据的有效性,舍去第3组数据,然后求出1、2组平均消耗V(NaOH),接着根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$来计算.
解答 解:(1)碱式滴定管在装液前应用所装液体进行润洗,用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上,碱式滴定管未用标准盐酸溶液润洗就直接注入标准NaOH溶液,标准液的浓度偏小,造成V(标准)偏大,根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析,可知c(标准)偏大;
故答案为:①;偏大;
(2)步骤⑤中,在记录滴定管液面读数时,滴定管尖嘴有气泡,造成V(标准)偏小,根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析,可知c(标准)偏小,故答案为:偏小;
(3)滴定结束前,锥形瓶中滴入酚酞,溶液为无色,滴定结束后,滴入氢氧化钠溶液后,溶液显示粉红色,所以达到终点的现象为:锥形瓶中溶液无色变为粉红,半分钟内不变色,
故答案为:无色变为粉红,半分钟内不变色;
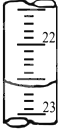
(4)滴定管中的液面读数为22.60mL,故答案为:22.60;
(5)三次滴定消耗的体积为:20.00mL,20.00mL,22.10,舍去第3组数据,然后求出1、2组平均消耗V(NaOH)=20.00mL,c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$=$\frac{0.2000mol•{L}^{-1}×20.00mL}{20.00mL}$=0.2000mol•L-1;
故答案为:0.2000.
点评 本题考查了酸碱中和滴定,题目难度不大,注注意把握中和滴定的原理、基本操作和误差分析的方法.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 丙醇与乙酸的反应条件通常是浓硫酸、加热 | |
| B. | 充分反应可以生成1mol乙酸乙酯 | |
| C. | 生成的乙酸丙酯和水的物质的量之比是1:2 | |
| D. | 反应结束时,剩余2mol乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
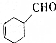 $→_{催化剂}^{H_{2}(足量)}$A$\stackrel{HBr}{→}$B$→_{干醚}^{Mg}$
$→_{催化剂}^{H_{2}(足量)}$A$\stackrel{HBr}{→}$B$→_{干醚}^{Mg}$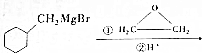 C$→_{Cu,△}^{O_{2}}$
C$→_{Cu,△}^{O_{2}}$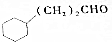 $→_{H+}^{KMnO_{4}}$D$→_{浓H_{2}SO_{4},△}^{E}$
$→_{H+}^{KMnO_{4}}$D$→_{浓H_{2}SO_{4},△}^{E}$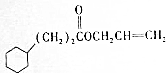
 RCH2CH2OH+
RCH2CH2OH+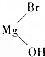
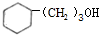 .
. 的化学方程式2
的化学方程式2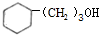 +O2$\stackrel{Cu}{→}$
+O2$\stackrel{Cu}{→}$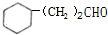 +2H2O,反应类型为氧化反应.
+2H2O,反应类型为氧化反应. ,反应类型为酯化反应.
,反应类型为酯化反应. ,名称为丙酮.
,名称为丙酮.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 测定序号 | 待测溶液的体积(mL) | 所耗盐酸标准液的体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铍(Be)的原子失电子能力比镁弱 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 氢氧化锶[Sr(OH)2]比氢氧化钙的碱性强 | |
| D. | 硒(Se)化氢比硫化氢稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
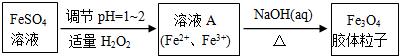
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe2+ | 5.8 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com