
已知:NaA的水溶液呈碱性。常温下将等体积的0.10 mol·L-1NaA溶液与0.05 mol·L-1 HCl溶液混合,所得溶液pH<7。据此判断以下说法不成立的是
A.c(Cl-)+c(OH-)+c(A-)>c(Na+) B.相同条件下HA的电离程度大于A-的水解程度
C.c(A-)+ c(HA)= c(Na+) D.c(A-)>c(Na+) >c(H+)>c(OH-)
科目:高中化学 来源:2016届宁夏银川市高三4月质检理综化学试卷(解析版) 题型:实验题
[化学 选修2:化学与技术]
铵盐是重要的化工原料,以N2和H2为原料制取硝酸铵的流程图如下,请回答下列问题:
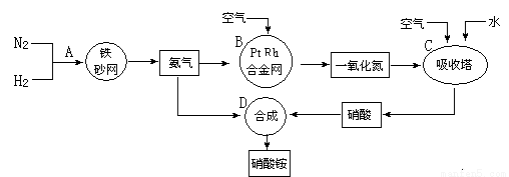
(1)在上述流程图中,B设备的名称是 ,其中发生反应的化学方程式为 。
(2)在上述工业生产中,N2与H2合成NH3的催化剂是 。1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如下:
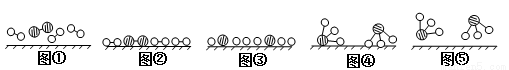
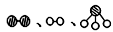 分别表示N2、H2、NH3 。图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是 、 。
分别表示N2、H2、NH3 。图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是 、 。
(3)NH3和CO2在一定条件下可合成尿素,其反应为:2NH3(g)+CO2(g)  CO( NH2)2(s)+H2O(g)
CO( NH2)2(s)+H2O(g)
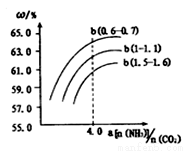
右图表示合成塔中氨碳比a与CO2转化率ω的关系。a为[n(NH3)/n(CO2)],b为水碳比[n(H2O)/n(CO2)]。则:
①b应控制在 ; A.1.5.1.6 B.1~1.1 C.0.6~0.7
②a应控制在4.0的理由是 。
(4)在合成氨的设备(合成塔)中,设置热交换器的目的是 ;在合成硝酸的吸收塔中通入空气的目的是 。
(5)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:NO+NO2+2NaOH=2NaNO2+H2O
NH3还原法:8NH3+6NO2 7N2+12H2O(NO也有类似的反应)
7N2+12H2O(NO也有类似的反应)
以上两种方法中,符合绿色化学的是 。
(6)某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量占总耗NH3质量(不考虑其它损耗)的 %。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三下学期考前练习化学试卷(解析版) 题型:实验题
【实验化学】
抗癌药物是己烷雌酚白色粉末,难溶于水,易溶于乙醇,它的一种合成原理如下:
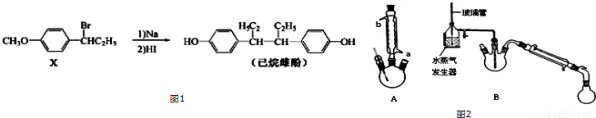 有关的实验步骤为(实验装置见图2):
有关的实验步骤为(实验装置见图2):
①向装置A中依次加入沸石、一定比例的试剂X和金属钠.
②控制温度300℃,使反应充分进行.
③向冷却后的三颈烧瓶内加入HI溶液,调节pH至4~5.
④在装置B中用水蒸气蒸馏,除去未反应的试剂X.
⑤…
(1)装置A中冷凝管由________端(填“a”或“b”)通入冷凝水.
(2)步骤③中反应的化学方程式为____________;
(3)装置B在进行水蒸气蒸馏之前,需进行的操作为___________,玻璃管的作用为_________________;
(4)当观察到装置B的冷凝管中____________________,说明水蒸气蒸馏结束.
(5)进行步骤⑤实验时,有下列操作(每项操作只进行一次):
a.过滤; b.加入水进行反萃取;c.冷却、抽滤,用水洗涤晶体;d.向三颈烧
瓶中加入乙醇,得己烷雌酚的乙醇溶液.正确的操作顺序是_________(填字母)。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三下学期考前练习化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为19。Y原子的电子层数与最外层电子数的比等于1/3,Z原子最外层电子数与内层电子数的比为1:10。下列说法正确的是
A.非金属性:Y<X<W
B.简单气态氢化物的热稳定性:Y<X
C.化合物ZW、XY中化学键类型相同
D.X、W的最高价氧化物的水化物均为强酸
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川二中高三三模理综化学试卷(解析版) 题型:填空题
【化学-选修2:化学与技术】
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料采用硝酸铵氧化分解技术生产CuC1的工艺过程如下:
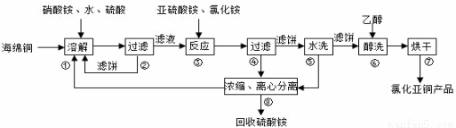
回答下列问题:
(1)步骤①中得到的氧化产物是___________,溶解温度应控制在60-70℃,原因是___________;
(2)写出步骤③中主要反应的离子方程式_________________;
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是__________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是_________________;
(5)步骤②、④、⑤、⑧都要进行固液分离.工业上常用的固液分离设备有_______(填字母)
A、分馏塔 B、离心机 C、反应釜 D、框式压滤机
(6)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amol/L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为___________。
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川二中高三三模理综化学试卷(解析版) 题型:选择题
化学与食品安全和环境保护息息相关,下列做法合理的是
A.食品加工,禁止使用化学添加剂
B.食品包装,用聚氯乙烯塑料
C.用塑化剂(树脂加工中添加剂)代替棕榈油作食品工业中的乳化剂,以节约加工成本
D.将地沟油回收加工为生物柴油。提高资源的利用率
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都石室中学高二4月月考化学试卷(解析版) 题型:选择题
在t℃时AgBr在水中的沉淀溶解平衡曲线如图所示。t℃时AgCl的Ksp=4×10-10,下列说法不正确的是
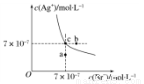
A.在t℃时,AgBr 的 Ksp为4.9×10-13
B.在 t ℃时,AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)的平衡常数 K≈816
AgBr(s)+Cl-(aq)的平衡常数 K≈816
C.图中a点对应的是AgBr的不饱和溶液
D.在 AgBr 饱和溶液中加入NaBr固体,可使溶液由c点变到b点
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都石室中学高二4月月考化学试卷(解析版) 题型:选择题
下列关于溶液中的离子共存问题或者离子反应的说法中正确的是
A.c(Fe3+) =0.1mol·L -1的溶液中:K+、NH4+、CO32-、SO42-能共存
B.与Al反应产生H2的溶液中, NO3-、Na+ 、SO42- 、Fe2+一定不共存
C.NaClO溶液中通入少量SO2:2ClO-+SO2 +H2O===SO32-+2HClO
D.用铜作电极电解NaCl溶液:2H2O+2Cl- Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:选择题
下列说法错误的是
A.葡萄糖可用于合成葡萄糖酸钙口服液
B.工业制普通玻璃的原料是石英、纯碱、石灰石
C.月饼包装盒中常放入生石灰或硅胶做干燥剂,铁粉或硫酸亚铁做抗氧化剂
D.原子利用率=期望产物的原子总数与生成物原子总数之比
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com