
| A. | 在一定温度下AgCl水溶液中,Ag+和Cl- 浓度的乘积是一个常数 | |
| B. | AgCl的Ksp=1.8×10-10,在任何含AgCl固体的溶液中,c(Ag+)=c(Cl- )且Ag+与Cl-浓度的乘积等于1.8×10-10 | |
| C. | 在一定温度下,向饱和AgCl水溶液中加入盐酸,Ksp值变大 | |
| D. | 在一定温度下,当溶液中Ag+和Cl- 浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液 |
分析 A.难溶电解质的饱和溶液中Ksp为定值;
B.硝酸银、盐酸等均可抑制AgCl固体的溶解;
C.Ksp只与温度有关;
D.饱和溶液中Ksp=c(Ag+)c(Cl- ),Qc>Ksp有沉淀析出,Qc<Ksp不生成沉淀.
解答 解:A.难溶电解质的饱和溶液中Ksp为定值,若不是饱和溶液,则Ag+和Cl- 浓度的乘积不是常数,故A错误;
B.硝酸银、盐酸等均可抑制AgCl固体的溶解,则Ag+与Cl-浓度的乘积等于1.8×10-10,c(Ag+)与c(Cl- )不一定相等,故B错误;
C.Ksp只与温度有关,则一定温度下,向饱和AgCl水溶液中加入盐酸,溶解平衡逆向移动,但Ksp值不变,故C错误;
D.在一定温度下,当溶液中Ag+和Cl- 浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液,达到沉淀溶解平衡,为动态平衡,故D正确;
故选D.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握Ksp与饱和溶液、温度的关系为解答的关键,侧重分析与应用能力的考查,注意Ksp只与温度有关,选项A为易错点,题目难度不大.


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ | |
| B. | 钠和冷水反应:Na+2H2O=Na++OH-+H2↑ | |
| C. | 将氯气溶于水制备次氯酸:Cl2+H2O=2H++Cl-+ClO- | |
| D. | 氢氧化钡溶液与稀硫酸反应:SO42-+Ba2+=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2CO3 NaHCO3 NaCl NH4Cl | |
| B. | Na2CO3 NaHCO3 NH4Cl NaCl | |
| C. | (NH4)2SO4 NH4Cl NaNO3 Na2CO3 | |
| D. | (NH4)2SO4 NH4Cl NaNO3 Na2S |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 符合条件 | 对应物质 |
| 混合物 | |
| 电解质,但熔融状态下不导电 | |
| 电解质,但难溶于水 | |
| 单质,本身能导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b=c | B. | c>a>b | C. | c>b>a | D. | b>c>a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 布朗运动不是胶体微粒特有的运动方式 | |
| B. | 光线透过胶体时,发生丁达尔效应,是因为粒子对光的散射造成的 | |
| C. | 胶体粒子能透过滤纸,所以不能用过滤的方法分离胶体和溶液 | |
| D. | 胶体能发生电泳,所以胶体带电荷,不在呈现电中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
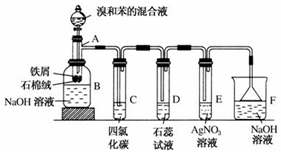 苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑.
苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑.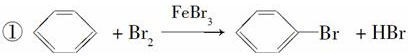 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com