
| A. | 溶液与胶体的本质区别是丁达尔效应 | |
| B. | 存放碳酸钠溶液的试剂瓶应使用玻璃塞 | |
| C. | 硝酸存放于棕色瓶中 | |
| D. | 试管、坩埚、蒸馏烧瓶都可以用酒精灯直接加热 |
分析 A.分散系的本质区别是分散质粒子的大小;
B.碳酸钠溶液水解显碱性,玻璃中二氧化硅会和碱发生反应;
C.硝酸见光易分解;
D.蒸馏烧瓶需要垫石棉网.
解答 解:A.胶体与溶液的本质区别是分散质粒子的大小,溶液(小于1nm)、胶体(1nm~100nm),故A错误;
B.碳酸钠溶液显碱性,能与玻璃塞中的二氧化硅反应而黏住,所以不能盛放在带有玻璃塞的试剂瓶中,故B错误;
C.硝酸见光分解,需要避光保存,存放于棕色瓶中,故C正确;
D.试管、坩埚都可以用酒精灯直接加热,蒸馏烧瓶属于大面积玻璃容器加热需要垫石棉网,故D错误;
故选C.
点评 本题考查了胶体组成、性质和本质、试剂存放、仪器使用等知识点,掌握基础是解题关键,题目难度不大.


 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①②③ | C. | ①②④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Na+、Cl-、OH- | B. | Fe2+、Mg2+、SO42-、Cl- | ||
| C. | K+、Na+、CO32-、OH- | D. | Na+、Ba2+、HCO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

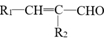 +H2O
+H2O +R2-OH$\stackrel{一定条件}{→}$
+R2-OH$\stackrel{一定条件}{→}$ +HCl
+HCl .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸光照变黄,证明硝酸不稳定,且产物有红棕色气体可溶于浓硝酸 | |
| B. | 向某溶液中加入氯化钡溶液和稀硝酸,生成白色沉淀,则原溶液一定含有硫酸根 | |
| C. | 常温下,将铝片放入浓硫酸中无明显现象,说明铝不与浓硫酸反应 | |
| D. | 溴水中通入SO2后,颜色褪去,说明SO2表现了漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙溶于稀盐酸中:CO32-+2H+═H2O+CO2↑ | |
| B. | 氯化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ | |
| C. | 铁与稀盐酸反应:2Fe+6H+═3H2↑+2Fe3+ | |
| D. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑧ | B. | ③⑥⑨⑩ | C. | ④⑤⑥⑧ | D. | ④⑤⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2是还原产物 | |
| B. | 有 0.250 mol KNO3 被氧化 | |
| C. | NaN3中氮元素为-3 价 | |
| D. | 被氧化的 N 原子的物质的量为 3.75mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水的颜色呈浅黄绿色,是因为氯水中含有Cl2 | |
| B. | 新制氯水能使红色布条褪色,说明氯水中含HClO | |
| C. | 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ | |
| D. | 活性炭和氯水都具有漂白作用,且漂白的化学原理相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com