
��һ���¶��£����Ϊ2L���ܱ������У�NO2��N2O4֮�䷢����Ӧ��2NO2 ��g�� ������ɫ��═N2O4��g�� ����ɫ������ͼ��ʾ��
��1����������Ӧ�ڼס���������ͬ������ͬʱ���У��ֱ��ü���v��NO2��=18mol/��L•min��������v��N2O4��=0.2mol/��L•s���������з�Ӧ���죮
��2����0��1min������X��ʾ�÷�Ӧ�������� ���÷�Ӧ����ʱ��Y��ת����60%����Ӧ��ʼʱ�뷴Ӧ��ƽ��״̬ʱ��ѹǿ֮��Ϊ ��
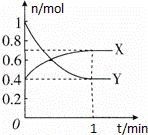
���㣺 ��ѧƽ�⽨���Ĺ��̣���ѧƽ���Ӱ�����أ�
������ ��1�����ݷ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȱȽϣ�
��2������v=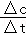 ���㷴Ӧ���ʣ����ͼ����������������
���㷴Ӧ���ʣ����ͼ����������������
��� �⣺��1������v��NO2��=18mol/��L•min��������v ��N2O4��=0.2mol•L﹣1•min﹣1��v��NO2��=2v��N2O4��=0.4mol•L﹣1•s﹣1=24mol/��L•min�������ҷ�Ӧ�Ͽ죬
�ʴ�Ϊ���ң�
��2��v��X��=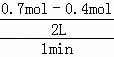 =0.15mol•��L•min��﹣1��
=0.15mol•��L•min��﹣1��
�÷�Ӧ�������ʱ��Y��ת����Ϊ��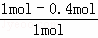 =60%��
=60%��
��ʼʱ��n��X��+n��Y��=0.4mol+1mol=1.4mol��
ƽ��ʱ��n��X��+n��Y��=0.7mol+0.4mol=1.1mol��
����ͬ�����£������ѹǿ֮�ȵ������ʵ���֮�ȣ�
��Ӧ��ʼʱ�뷴Ӧ��ƽ��״̬ʱ��ѹǿ֮��Ϊ1.4mol��1.1mol=14��11��
�ʴ�Ϊ��0.1mol•��L•min��﹣1��60%��14��11��
������ ���⿼���Ϊ�ۺϣ���Ŀ�Ѷ��еȣ�ע����ջ�ѧ��Ӧ�����Լ���ѧƽ��Ļ���֪ʶ���ɽ����⣮


 100�ִ�����ĩ���ϵ�д�
100�ִ�����ĩ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ԫ�ؿ����γ�AB2���ۻ�������ǣ���
A�� �����ӵ�ԭ�����������6�����ӵĶ�����Ԫ�ص�ԭ��
B�� �˵�����ֱ�Ϊ12��17��Ԫ��
C�� ��A��͢�A��ԭ�Ӱ뾶��С��Ԫ��
D�� ������۶�Ϊ���������ֶ�����Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1����Ҫ����100mL0.1mol•L﹣1Na2SO4��Һ�������Na2SO4������Ϊ1.4g��
��2����2240mL����ȫ����ˮ���100mL��Һ����ˮ��NH3�����ʵ���Ũ��Ϊ1mol•L﹣1����������NH3��H2O�ķ�Ӧ��
��3��ʵ�����ﳣ�ù����Ȼ����������ʯ�Ҽ�����ȡ��������Ҫ2240mL����״����������������Ҫ�Ȼ�淋�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ӦH2��g��+I2��g��⇌2HI��g��������̶����ܱ������н��У��ﵽƽ��״̬�ı�־�ǣ���
�ٵ�λʱ���ڶ���n mol H﹣H����ͬʱ�γ�2n mol H﹣I��
�ڵ�λʱ��������n molI2��ͬʱ����2n molHI
��2v����H2��=v����HI��
��HI���������ٸı�
�ݻ��������ɫ���ٸı�
�������ѹǿ���ٸı䣮
A�� �ڢܢݢ� B�� �ڢۢܢ� C�� �٢ۢܢ� D�� ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪ijԪ�ص�������R2+�ĺ���������Ϊn��������ΪA����mg�������������������ӵ����ʵ����ǣ���
A�� 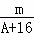 ��A﹣n+8��mol B��
��A﹣n+8��mol B�� 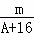 ��A﹣n+10��mol
��A﹣n+10��mol
C�� ��A﹣n+2��mol D�� 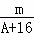 ��A﹣n+6��mol
��A﹣n+6��mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ����������ݺ������ǣ���
A�� ��10 mL ��Ͳ��ȡ5.2 mL����
B�� �ù㷺pH��ֽ���ij��Һ��pHֵΪ12.5
C�� ��������ƽ��ȡ25.12gNaCl����
D�� ��100 mL����ƿ����50mL0.1 mol/L������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������O2��O3����
A�� ����ԭ������ͬ
B�� ������������ͬ
C�� ͬ��ͬѹ�£����������ͬ
D�� ͬ��ͬѹ�£�������ܶ���ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͬ�¡�ͬѹ�£�������ȵ�SO2��CO2��Ƚϣ����֮��Ϊ ��
��֪SO2��CO2��Ϊ���������д��CO2������NaOH��Һ��Ӧ�����ӷ���ʽ ��
��ij��Һ�п��ܺ��д������������ӣ�OH﹣��SO42﹣��CO32﹣��Cl﹣��
��1������Һ�д��ڴ���H+ʱ������Һ�в������� ��
��2������Һ���д�����Ba2+����ʱ������Һ�в������� �������ӷ���ʽд�������ܴ��ڵ�ԭ�� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������������Ρ����������ͱ����ߺ�ߣ���ͼ��Ԫ�����ڱ��ṩ�IJ�Ԫ�صIJ�����Ϣ�������йز���˵���в���ȷ���ǣ�������
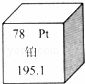
| �� | A�� | ԭ��������78 | B�� | ���ڷǽ���Ԫ�� |
| �� | C�� | Ԫ�ط�����Pt | D�� | ���ԭ��������195.1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com