
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。请回答下列问题:
(1)工业上采用电解氧化铝-冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝:
2Al2O3  4Al+3O2↑加入冰晶石的作用:_______________________________。
4Al+3O2↑加入冰晶石的作用:_______________________________。
(2)上述工艺所得铝材中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为 ,下列可作阴极材料的是________________。
A.铝材 B.石墨 C.铅板 D.纯铝
 (3)阳极氧化能使金属表面生成
(3)阳极氧化能使金属表面生成
致密的氧化膜。以稀硫酸为电解液,铝
阳极发生的电极反应式为
__________________________________。
(4)在铝阳极氧化过程中,需要不断
地调整电压,理由是____________ ___
。
(5)下列说法正确的是 。
A. 阳极氧化是应用原电池原理进行金属材料表面处理的技术
B. 铝的阳极氧化可增强铝表面的绝缘性能
C. 铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
D. 铝的阳极氧化膜富有多孔性,具有很强的吸附性能,能吸附染料而呈各种颜色
科目:高中化学 来源: 题型:
自然界中存在大量的金属元素,其中钠、镁、铁、铜等在工农业生产中有着广泛的应用。
(1)合成氨是人类科学技术上的一项重大突破,工业合成氨生产中常用铁触媒作催化剂。请写出Fe元素的基态原子核外电子排布式 。
(2)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac— = CH3COO—),其反应是:
[Cu(NH3)2] Ac +CO+NH3  [Cu(NH3)3]Ac·CO[醋酸羰基三氨合铜(I)] △H<0
[Cu(NH3)3]Ac·CO[醋酸羰基三氨合铜(I)] △H<0
①C、N、O三种元素的第一电离能由小到大的顺序为 。
②[Cu(NH3)2]+中存在的化学键类型有 (填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
③氨分子中N原子的杂化方式为 。
 (3)NaCl和MgO都属离子化合物,NaCl的熔点为801.3℃, MgO的熔
(3)NaCl和MgO都属离子化合物,NaCl的熔点为801.3℃, MgO的熔
点高达2800℃。造成两种晶体熔点差距的主要原因是 。
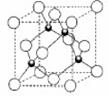
(4)铜的化合物种类也很多,其常见价态为+1、+2价。如CuO、Cu2O、
CuH等。右图是铜的一种氯化物晶体的晶胞结构,则它的化学式是
。
查看答案和解析>>
科目:高中化学 来源: 题型:
有50ml0.1mol/L碘水,当通入足量Cl2完全反应后,共转移了0.05mol电子,则下列叙述错误的是
A.该反应中H2O是反应物之一 B.氧化剂与还原剂的物质的量之比为1∶5
C.氧化产物为HIO3 D.若有1 mol I2参加氧化反应,转移10 mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的数值,下列说法正确的是 ( )
A、标准状况下,11.2 L SO3所含的原子数为2NA
B、标准状况下,22.4L氧气和乙炔混合物所含的分子数为NA
C、23 g钠在氧气中完全燃烧失电子数为0.5 NA
D、100 mL 2.0 mol/L的Na2S溶液中S2-离子个数等于0.2 NA 
查看答案和解析>>
科目:高中化学 来源: 题型:
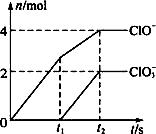
向一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示。已知,生成ClO3-的反应为:6Ca(OH)2+6Cl2  5CaCl2+Ca(ClO3)2+6H2O。
5CaCl2+Ca(ClO3)2+6H2O。
试回答:
(1)t2时,Ca(ClO)2与Ca(ClO3)2的物质的量之和为_________ mol,该石灰乳中含有的Ca(OH)2的质量是_________ g。
(2)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入氯气的速率不同,n(ClO-)和n (ClO3-)的比例也不同。若在原石灰乳中通入氯气的速率加快,则反应后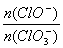 _____2(填“>”“<”或“=”)。
_____2(填“>”“<”或“=”)。
(3)若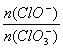 =a,则n(Cl-)=_________ mol(用含a的代数式表示)。
=a,则n(Cl-)=_________ mol(用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列九种物质:①H2 ②铝 ③CuO ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO4)3
(1)按物质的分类方法填写表格的空白处:
| 分类标准 | 能导电 | 非电解质 | 电解质 |
| 属于该类的物质 |
|
|
|
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com