
分析 (1)混合气体的密度是相同状况下H2密度的12.5倍,所以混合物的平均摩尔质量为12.5×2g/mol=25g•mol-1,所以混合气体中一定有甲烷,混合气体的总的物质的量为:$\frac{10g}{25g/mol}$=0.4mol,该混合气通过Br2水时,Br2水增重8.4g,8.4g为烯烃的质量,所以甲烷的质量为10g-8.4g=1.6g,则甲烷的物质的量为:$\frac{1.6g}{16g/mol}$=0.1mol,故烯烃的物质的量为:0.4mol-0.1mol=0.3mol,由此分析解答;
(2)CH4燃烧产物为CO、CO2、H2O(g),产物通过无水CaCl2时,无水CaCl2的作用是吸收水分,无水CaCl2增重22.5g为水的质量,根据H原子守恒可计算CH4的物质的量,根据C原子守恒可计算CO和CO2的总的物质的量,再根据二者质量可计算CO2的物质的量,进而计算CO2质量.
解答 解:(1)混合气体的密度是相同状况下H2密度的12.5倍,所以混合物的平均摩尔质量为12.5×2g/mol=25g•mol-1,所以混合气体中一定有甲烷,混合气体的总的物质的量为:$\frac{10g}{25g/mol}$=0.4mol,该混合气通过Br2水时,Br2水增重8.4g,8.4g为烯烃的质量,所以甲烷的质量为10g-8.4g=1.6g,则甲烷的物质的量为:$\frac{1.6g}{16g/mol}$=0.1mol,故烯烃的物质的量为:0.4mol-0.1mol=0.3mol,烷烃与烯烃的体积比为:1:3,
故答案为:1:3;
(2)产物通过无水CaCl2时,无水CaCl2增重25.2g为水的质量,
所以n(H2O)=$\frac{22.5g}{18g/mol}$=1.25mol,
根据H原子守恒,可知:n(CH4)=$\frac{1}{2}$n(H2O)=$\frac{1}{2}$×1.25mol=0.625mol,
根据C原子守恒,则:n(CO)+n(CO2)=0.0.625mol,
根据混合物总质量可知:m(CO)+m(CO2)=49.6g-22.5g=27.1g,
则:[0.625mol-n(CO2)]×28g/mol+n(CO2)×44g/mol=27.1g,
解得:n(CO2)=0.6mol,
所以生成二氧化碳的质量为:0.6mol×44g/mol=26.4g,
故答案为:26.4 g.
点评 本题考查混合物的计算,题目难度中等,明确发生反应的实质为解答关键,注意从原子守恒的角度解答,关键根据水的质量判断甲烷的物质的量,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
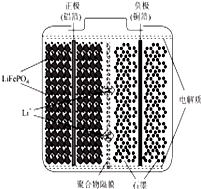 锂离子电池广泛应用与日常电子产品中,也是电动汽车动力电池的首选.正极材料的选择决定了锂离子电池的性能.磷酸亚铁锂(LiFePO4)以其高倍率性、高比能量、高循环特征、高安全性、低成本、环保等优点而逐渐成为“能源新呈”.
锂离子电池广泛应用与日常电子产品中,也是电动汽车动力电池的首选.正极材料的选择决定了锂离子电池的性能.磷酸亚铁锂(LiFePO4)以其高倍率性、高比能量、高循环特征、高安全性、低成本、环保等优点而逐渐成为“能源新呈”.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期第0族 | B. | 第四周期第ⅠA族 | C. | 第三周期第ⅠA族 | D. | 第三周期第ⅦA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原溶液中肯定不含Fe2+、NO3-、SiO32-、I- | |
| B. | 原溶液中肯定含有K+、Fe3+、Fe2+、NO3-、SO42- | |
| C. | 步骤Ⅱ中无色气体是NO气体,无CO2气体产生 | |
| D. | 为确定是否含有Cl-可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不慎打翻燃着的酒精灯,立即用湿抹布盖灭 | |
| B. | 实验室制取氯气如果有尾气处理装置,可不用在通风橱中进行 | |
| C. | 给盛有液体的试管加热时,要不断移动试管或加入碎瓷片 | |
| D. | 浓碱液滴在皮肤上,立即用大量水冲洗,然后涂上硼酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 《西游记》中孙悟空一个“筋头云”,十万八千里,其乃“腾云驾雾”而行,其中的云不是胶体,雾是胶体 | |
| B. | 《水浒》中经典片段-----智劫生辰纲中,晁盖等人用蒙汗药药倒杨智等人.其使用的蒙汗药的主要成份可能是NaCN | |
| C. | 《三国演义》中,诸葛亮擒拿南王孟获时路遇哑泉,人饮用了哑泉水后,一个个说不出话来,其主要成份是CuSO4.智者指教,饮安乐泉水可解毒,安乐泉水主要成份可能是氢氧化钙 | |
| D. | 《红楼梦》中有经典语句:女儿是水做的骨肉,男人是泥做的骨肉.水分子间通过氢键结合而质软,泥因其主要成分是碳酸钙而质硬.这句话借此形容男女的性格差异 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
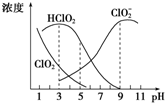 亚氯酸钠是一种高效氧化剂、漂白剂,主要用于棉纺、纸浆等漂白,亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO${\;}_{2}^{-}$、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列分析错误的是( )
亚氯酸钠是一种高效氧化剂、漂白剂,主要用于棉纺、纸浆等漂白,亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO${\;}_{2}^{-}$、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列分析错误的是( )| A. | 亚氯酸钠在碱性条件下较稳定 | |
| B. | 25℃时,HClO2的电离平衡常数的数约为Ka=10-6 | |
| C. | 25℃时,同浓度的HClO2溶液和NaClO2溶液等体积混合(忽略Cl-),则混合溶液中有c(HClO2)+2c(H+)═c(ClO${\;}_{2}^{-}$)+2c(OH-) | |
| D. | 使用该漂白剂的最佳pH为3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com