
【题目】下列反应的离子方程式正确的是
A.FeCl3溶液与Cu的反应:Fe3++Cu=Fe2++Cu2+
B.AgNO3溶液与NaCl溶液的反应:Ag++Cl-=AgCl↓
C.Cu(OH)2与CH3COOH溶液的反应:OH-+H+=H2O
D.CaCO3与HNO3溶液的反应:![]() +2H+=H2O+CO2↑
+2H+=H2O+CO2↑
科目:高中化学 来源: 题型:
【题目】锌是人体必需的微量元素,明朝《天工开物》中有世界上最早的关于炼锌技术的记载。回答下列问题:
(1)基态Zn原子的价电子排布式为____________,在周期表中位置为________________。
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①组成[Zn(NH3)4]SO4的元素中,除H外其余元素的第一电离能由大到小排序为________________________。
②在[Zn(NH3)4]SO4溶液中滴加NaOH溶液,未出现浑浊,其原因是___________________________。
③已知[Zn(NH3)4]2+的空间构型与SO42-相同,则在[Zn(NH3)4]2+中Zn2+的杂化类型为________。
④以下作用力在[Zn(NH3)4]SO4晶体中存在的有________。
A.离子键 B.极性共价键 C.非极性共价键
D.配位键 E.范德华力 F.金属键
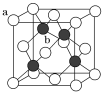
(3)ZnS晶胞结构如图(已知a为硫离子,b为锌离子)所示,ZnS晶体的熔点约为1 700 ℃。
①已知晶体密度为ρ g·cm-3,NA为阿伏加德罗常数的值。则1个ZnS晶胞的体积为________cm3。
②ZnO与ZnS结构相似,熔点为1 975 ℃,其熔点较高的原因是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十九大报告中提出要“打赢蓝天保卫战”,意味着对污染防治比过去要求更高。某种利用垃圾渗透液实现发电、环保二位一体结合的装置示意图如下,当该装置工作时,下列说法正确的是
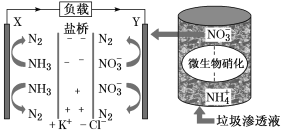
A.盐桥中Cl-向Y极移动
B.电路中流过7.5 mol电子时,共产生标准状况下N2的体积为16.8L
C.电流由X极沿导线流向Y极
D.Y极发生的反应为2NO3-+10e-+6H2O===N2↑+12OH—,周围pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是
A.再通入少量氯气,c(H+)/c(ClO-)减小
B.通入少量SO2,溶液漂白性增强
C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
D.加入少量水,水的电离平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.常温下,1mol·L-1的CH3COOH溶液与1mol·L-1的NaOH溶液等体积混合后,所得混合液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B.在含有酚酞的0.1mol/L氨水中加入少量的NH4Cl晶体,溶液颜色变浅
C.氢硫酸的电离方程式为:H2S![]() 2H++S2﹣
2H++S2﹣
D.0.1mol/LNa2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素。Y和W的最外层电子数都是1,Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍,且X与Z同主族。由此可知:
(1)写出元素符号:W为_________,Z为_________
(2)W2X是由_________键组成的分子,其电子式为_________
(3)写出Y的最高价氧化物对应水化物与Z的最高价氧化物对应水化物反应的离子方程式_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是
①KHCO3 ②(NH4)2CO3③Al2O3④Al(OH)3
A.全部B.只有①③④C.只有③④D.只有②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组设计如图装置(部分夹持装置已略去),以探究潮湿的Cl2与Na2CO3反应得到固体物质的成分。
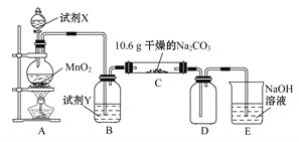
(1)试剂X的化学式________。A中制取Cl2的离子方程式____________________。
(2)试剂Y的名称为______________。
(3)通入一定量潮湿的Cl2反应后,经检测,D中只有Cl2O一种气体,C中除含一种氯盐外,同时含有NaHCO3等,某同学对C中所得固体残渣的成分进行探究。
①提出合理假设。
假设1:存在两种成分:NaHCO3和____________________________;
假设2:存在三种成分:NaHCO3和__________________________。
②设计方案,进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯。
实验步骤 | 预期现象和结论 |
步骤1:取C中的少量固体样品于试管中,滴加足量蒸馏水至固体溶解,然后将所得溶液分别置于A、B试管中 | |
步骤2:向A试管中滴加BaCl2溶液 | __________________ |
步骤3:______________ | __________________ |
(4)已知Cl2O与水反应生成次氯酸,则D中Cl2O进入E反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应2SO2+O2![]() 2SO3的叙述不正确的是( )
2SO3的叙述不正确的是( )
A.该反应是可逆反应,在相同条件下,反应可同时向两个方向进行
B.1mol氧气与2mol二氧化硫混合发生反应能生成2mol三氧化硫
C.在该反应中二氧化硫作还原剂,氧气作氧化剂
D.该反应有0.4mol电子发生转移时,生成三氧化硫0.2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com