
| A、氧化性由强到弱的顺序为KBrO3>KClO3>Cl2>Br2 |
| B、①中KCl是氧化产物,KBr 发生还原反应 |
| C、③中2mol氧化剂参加反应得到电子的物质的量为10 mol |
| D、反应②中氧化剂与还原剂的物质的量之比为1:6 |


科目:高中化学 来源: 题型:
| A、②④ | B、①③ | C、①⑤ | D、③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X是H2O |
| B、还原性:SO42->Mn2+ |
| C、该反应中酸性介质可以为盐酸 |
| D、每生成0.1molSO42-,转移电子0.05mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a=4 | ||
| B、每有1molO2参加反应,转移的电子总数为4mol | ||
| C、只有S2O32-是还原剂 | ||
D、Fe2+中有
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 金属 | Na | Cu | Al | Fe |
| 熔点(℃) | 97.5 | 1 083 | 660 | 1 535 |
| 沸点(℃) | 883 | 2 595 | 2 200 | 3 000 |
| A、Cu与Al |
| B、Fe与Cu |
| C、Fe与Na |
| D、Al与Na |
查看答案和解析>>
科目:高中化学 来源: 题型:
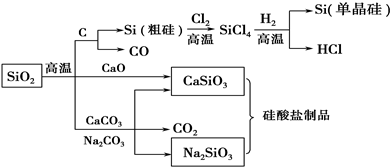
| A、高炉炼铁时,加入石灰石将铁矿石中的脉石(主要成分为SiO2)转化为易熔的炉渣 |
| B、纯净的二氧化硅和单晶硅都是信息产业的重要基础材料 |
| C、用盐酸可除去石英砂(主要成分为SiO2)中少量的碳酸钙 |
| D、图中所含反应都不属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、SO42-、Br-、SiO32- |
| B、H+、Fe2+、Cl-、NH4+ |
| C、Na+、Ba2+、NO3-、Cl- |
| D、Na+、Ag+、NH3?H2O、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3Cl2+6FeI2═2FeCl3+4FeI3 |
| B、Cl2+FeI2═FeCl2+I2 |
| C、Co2O3+6HCl═2CoCl2+Cl2↑+3H2O |
| D、2Fe3++2I-═2Fe2++I2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com