
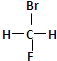 和
和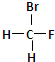 ②1H-、2H、3H+、D2 ③淀粉和纤维素 ④
②1H-、2H、3H+、D2 ③淀粉和纤维素 ④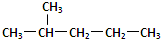 和
和 ⑤16O2、18O3 ⑥235U、238U
⑤16O2、18O3 ⑥235U、238U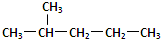 和
和 分子式相同结构不同,互为同分异构体;
分子式相同结构不同,互为同分异构体;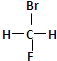 和
和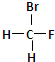 分子式相同,结构相同,是同一种化合物;
分子式相同,结构相同,是同一种化合物;

科目:高中化学 来源: 题型:
| A、铁片溶于硫酸铜溶液中:Fe+Cu2+═Cu+Fe2+ | ||
B、氢氧化钡溶液与稀硫酸混合:H++
| ||
| C、硫酸氢钠溶液与NaOH溶液混合:H++OH-═H2O | ||
| D、向硫酸铜溶液中加入Na2S溶液:Cu2++S2-═CuS↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)氢是未来最好的能源选择,制取氢气的成熟的方法有很多,利用甲醇可以与水蒸气反应生成氢气,反应方程式如下:
(1)氢是未来最好的能源选择,制取氢气的成熟的方法有很多,利用甲醇可以与水蒸气反应生成氢气,反应方程式如下:查看答案和解析>>
科目:高中化学 来源: 题型:
 维生素C主要存在于蔬菜、水果中,它能增加人体对疾病的抵抗能力.其结构简式如图,请回答:
维生素C主要存在于蔬菜、水果中,它能增加人体对疾病的抵抗能力.其结构简式如图,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
23 11 |
1 1 |
2 1 |
3 1 |
1 1 |
2 1 |
3 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 溶液组成主要成分 | 对应图象 | 溶液中离子浓度关系 | |
| A | NaHCO3、Na2CO3 | Ⅱ | c(CO32-)<c(HCO3-) |
| B | NaOH、Na2CO3 | Ⅳ | c(OH-)>c(CO32-) |
| C | Na2CO3 | Ⅲ | c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| D | NaHCO3 | I | c(Na+)=c(HCO3-) |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com