
【题目】欲将蛋白质从水中析出而又不改变它的性质,应加入 ( )
A. (NH4)2SO4溶液 B. 75%的酒精溶液
C. CuSO4溶液 D. NaOH浓溶液
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源、环保等方面有着广泛的用途。湿法、干法制备高铁酸盐的原理如下表所示。
湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如下图所示:
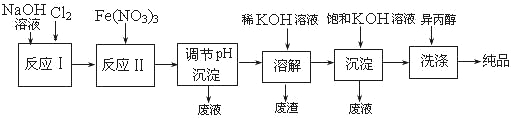
①洗涤粗品时选用异丙醇而不用水的理由是: 。
②反应Ⅱ的离子方程式为 。
③高铁酸钾在水中技能消毒杀菌,又能净水,是一种理想的水处理剂,它能消毒杀菌是因为 ,它能净水的原因是因为 。
④已知25℃时Fe(OH)3的Ksp = 4.0×10-38,反应II后的溶液c(Fe3+)=4.0×10-5mol/L,则需要调整到 时,开始生成Fe(OH)3(不考虑溶液体积的变化)。
(2)由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠中加入饱和KOH溶液,即可析出高铁酸钾。
①加入饱和KOH溶液的目的是 。
②由以上信息可知:高铁酸钾的溶解度比高铁酸钠 (填“大”或“小”)。
(3)干法制备K2FeO4的反应中氧化剂与还原剂的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列各组物质按酸、碱、盐分类顺次排列,正确的是( )
A. 硫酸、纯碱、石膏 B. 硫酸、烧碱、绿矾
C. 硫酸氢钠、生石灰、醋酸钠 D. 磷酸、熟石灰、苛性钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高分子树脂M具有较好的吸水性,其合成路线如下:

已知: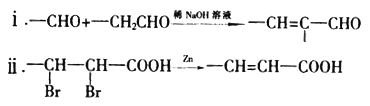
(1)C的名称为______________,D中的官能团为__________________,结构简式为_____________。
(2)由A生成B的化学方程式为___________________。
(3)上述合成路线中,D→E转化在合成M中的作用为___________________________。
(4)下列关于F的叙述正确的是___________。
A.能与NaHCO3反应生成CO2 B.能发生水解反应和消去反应
C.能聚合成高分子化合物 D. 1 mol G最多消耗2 mol NaOH
(5)H是G的同系物,且与G相差一个碳原子,则同时满足下列条件的H的同分异构体共有______种(不考虑立体异构)。
①与G具有相同的官能团 ②苯环上只有两个取代基
(6)根据上述合成路线和信息,以苯乙醛为原料(其他无机试剂任选),设计制备 的合成路线_________________________。
的合成路线_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下述装置制取氯气,并用氯气进行下列实验。看图回答下列问题:

(1)A、B两仪器的名称:A________,B________。
(2)洗气装置C是为了除去Cl2中的HCl气体,D是为了干燥Cl2,则C、D中应分别放入下列溶液中的C______________;D______________。
①NaOH溶液 ②饱和食盐水 ③AgNO3溶液 ④浓H2SO4
(3)E 中为红色干布条,F 中为红色湿布条,可观察到的现象是_______________。
(4)G是浸有淀粉KI溶液的棉花球,G处现象是棉花球表面变成____________。反应的离子方程式是________________,H是浸有NaBr溶液的棉花球,H处现象是棉花球表面变成________。
(5)P处为尾气吸收装置,可选用下列装置中的 ____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面提供的仪器和试剂,完成验证SO2既有氧化性又有还原性的实验。已知:
①SO2+Br2+2H2O→2HBr+H2SO4;②FeS+2HCl→FeCl2+ H2S↑(FeS块状固体难溶于水)
可选用的仪器如图所示:
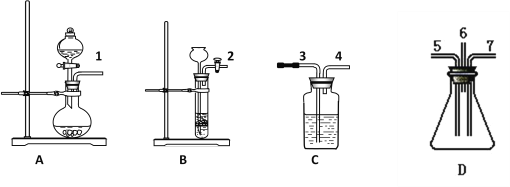
可选用的试剂:
①稀盐酸,②溴水,③Na2SO3粉末状固体,④FeS固体,⑤品红溶液,⑥氢氧化钠溶液,⑦浓硫酸。试回答下列问题:
(1)制取SO2气体选用装置____( 从A——D中选取,填字母),选用的试剂是____和______(从①——⑦中选取,填数字)。
(2) 制取H2S气体选用装置____( 从A——D中选取,填字母),选用的试剂是____和_____(从①——⑦中选取,填数字)。
(3)表现SO2氧化性的实验是上述仪器中的D装置,有关化学方程式是______________________;
表现SO2还原性的实验是上述仪器中的_______装置,能观察到的实验现象是_______________。
(4)为了防止污染空气,从装置D出气口排出的气体要用_____吸收(从①——⑦中选取,填数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com