
| A、Cl- |
| B、H+ |
| C、OH- |
| D、Na+ |


科目:高中化学 来源: 题型:
| 实验序号 | 加入试剂 | 实验现象 |
| Ⅰ | 4mL 2mol?L-1 HCl溶液 | 沉淀溶解 |
| Ⅱ | 4mL 2mol?L-1 NH4Cl溶液 | 沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、常温常压下,6 g
| ||
| B、标准状况下,0.3 mol二氧化硫中含有氧原子数为0.3NA | ||
| C、常温下,2.7 g铝与足量的盐酸反应,失去的电子数为0.3NA | ||
| D、常温下,1 L 0.1 mol/L MgCl2溶液中含Mg2+数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放电时负极附近溶液的pH不变 |
| B、放电时电解质溶液中的OH-向正极移动 |
| C、充电时电池的负极应与电源的负极相连接 |
| D、充电时阳极反应:Ni(OH)2-e-+OH-=NiOOH+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、操作和现象:切开金属钠,钠表面的银白色会逐渐变暗;结论:Na在空气中会生成Na2O2 | ||
| B、操作和现象:铝箔插入浓硝酸中,无明显现象;结论:铝与浓硝酸不反应 | ||
| C、操作和现象:SO2通入滴有酚酞的NaOH溶液,溶液褪色;结论:SO2具有漂白性 | ||
D、操作和现象:将充满NO2的试管倒立在水中,试管内液面约上升至试管容积的
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实 验 内 容 | 实 验 目 的 | |
| A | 将SO2通入酸性KMnO4溶液中 | 证明SO2的水溶液具有弱酸性 |
| B | 将饱和的FeCl3溶液滴到沸水中 | 促进Fe3+水解,制得Fe(OH)3胶体 |
| C | 在淀粉KI溶液中滴加少量市售食盐配制的溶液 | 真假碘盐的鉴别 |
| D | 在少量Fe(NO3)2试样加水溶解的溶液中,滴加稀H2SO4酸化,再滴加KSCN溶液 | 检验Fe(NO3)2试样是否变质 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
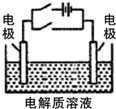
| A、阴极(Cu片):2C1--2e-=Cl2↑ |
| B、阳极(Cu片):4OH--4e-=2H2O+O2↑ |
| C、正极(石墨棒):Fe3++e-=Fe2+ |
| D、负极(Fe钉):Fe-3e-=Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
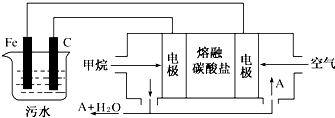
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com