
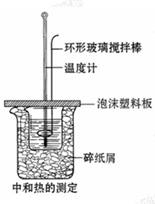
��16�֣���ͼ��ʾ:��800 mL�Ĵ��ձ��з�����ֽм����ʢ��50 mL 0.50 mol��L-1�����200 mL�ձ��ŵ����ձ��У���ֻ�ձ���������ֽм������ĭ���ϰ����ɴ��ձ��ǣ�ͨ�����Ӳ���һ��������������ĩ�˳ʰ�Բ���IJ���������һֻ�¶ȼƣ��ⶨ��Һ���¶ȡ�Ѹ����������Һ�м���50 mL 0.55 mol��L-1�ռ���Һ���Ǻã�������Һ���۲��¶ȵı仯�����¶ȱ����ȶ�ʱ����¼������ȡ��װ��ӦҺ���ձ���������Һ����ϴ�ɾ����������Ɑ�ڸ���ظ���������ʵ�顣����һʵ����Դ��Բⶨ�к��ȡ�
��1���ձ���������ֽм��������_____ ��
��2��Ҫ�ظ���������ʵ���Ŀ����_____ ��
��3���ձ��粻��Ӳֽ�壬��õ��к�����ֵ��_____ ���ƫ����ƫС������Ӱ�족����
��4��ʵ����������60 mL 0.50 mol��L-1�����50 mL 0.55 mol��L-1�ռ���Һ����������Ӧ��������ʵ����ȣ����ų�������_____ �����ȡ�����ȡ����������к���_____ �����ȡ�����ȡ�����������_____��
��5������ƽ�в�����������У���ʼʱ�������ռ���Һ�¶���ͬ������ֹ�¶�����ʼ�¶�֮�t2-t1���ֱ�Ϊ ��2.3 �桡��2.4 �桡��2.9 �棬�����մ������ʽ���¶Ȳ��ƽ��ֵΪ_____ �档
��1�����¡����ȡ�����ʵ������зų���������ʧ
��2������ʵ������е�������3��ƫС������4������ȡ���ȡ���Ϊ60 mL 0.50 mol��L-1�����50 mL 0.55 mol��L-1�ռӦ������0.027 5 mol H2O����50 mL 0.50 mol��L-1������50 mL 0.55 mol��L-1�ռӦֻ������0.025 mol H2O��������ų�������ͬ�����к�����ָ�������кͷ�Ӧ����1 mol H2Oʱ���ų������������ᡢ��������أ���������к�����ȡ���5��2.53
���������ⶨ�к��ȵ�ʵ����һ������ʵ�飬����ʵ��װ�úͲ���ʱҪע���������棺һ�ǡ����������⣬���Ǿ�������ʵ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ν��ʹ�����CO2�ĺ�������Ч�ؿ�������̼��Դ���о��Ե���Ϊ���ȣ�
��ν��ʹ�����CO2�ĺ�������Ч�ؿ�������̼��Դ���о��Ե���Ϊ���ȣ�| ���� |
| �¶�/k CO2ת����/% n��H2��/n��CO2�� |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
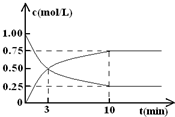
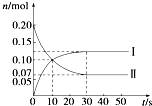 ���ݻ�Ϊ2L���ܱ������У�������ϵ���¶�800�治�䣬��һ������NO��O2��Ϸ�����Ӧ��2NO+O2?2NO2������NO�����ʵ�����n����ʱ�䣨t���ı仯��ϵ��ͼ��ʾ����ش��������⣮
���ݻ�Ϊ2L���ܱ������У�������ϵ���¶�800�治�䣬��һ������NO��O2��Ϸ�����Ӧ��2NO+O2?2NO2������NO�����ʵ�����n����ʱ�䣨t���ı仯��ϵ��ͼ��ʾ����ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
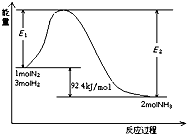 ��һ��������ܱ������У��������»�ѧ��Ӧ��
��һ��������ܱ������У��������»�ѧ��Ӧ��| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| [CO]?[H2O] |
| [CO2]?[H2] |
| [CO]?[H2O] |
| [CO2]?[H2] |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
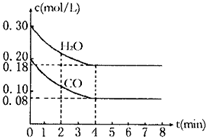
 CO��g��+H2O��g������Ӧ�ʱ�Ϊ��H���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO��g��+H2O��g������Ӧ�ʱ�Ϊ��H���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���| T�� | 700 | 800 | 850 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ����һ��ѧ���ڶ��¡���ѧ��Ӧ��������2.1����ѧ��������(�˽̰����2) ���ͣ�058
��ͼ��ʾ����800 mL�Ĵ��ձ��з�����ֽм����ʢ��50 mL��0.50 mol��L��1�����200 mL�ձ��ŵ����ձ��У���ֻ�ձ���������ֽм������ĭ���ϰ����ɴ��ձ��ǣ�ͨ�����Ӳ���һ������������(ĩ�˳ʰ�Բ���IJ�����)��һֻ�¶ȼƣ��ⶨ��Һ���¶ȣ�Ѹ����������Һ�м���50 mL��0.55 mol��L��1�ռ���Һ���Ǻã�������Һ���۲��¶ȵı仯�����¶ȱ����ȶ�ʱ����¼������ȡ��װ��ӦҺ���ձ���������Һ����ϴ�ɾ����������Ɑ�ڸ���ظ���������ʵ�飮����һʵ����Դ��Բⶨ�к��ȣ�
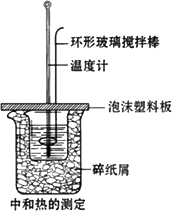
(1)�ձ���������ֽм��������________��
(2)Ҫ�ظ���������ʵ���Ŀ����________��
(3)�ձ��粻��Ӳֽ�壬��õ��к�����ֵ��________(�ƫ����ƫС������Ӱ�족)��
(4)ʵ����������60 mL��0.50 mol��L��1�����50 mL��0.55 mol��L��1�ռ���Һ����������Ӧ��������ʵ����ȣ����ų�������________(���ȡ�����ȡ�)�������к���________(���ȡ�����ȡ�)��������________��
(5)����ƽ�в�����������У���ʼʱ�������ռ���Һ�¶���ͬ������ֹ�¶�����ʼ�¶�֮��(t2��t1)�ֱ�Ϊ
��2.3��
��2.4��
��2.9�棬
�����մ������ʽ���¶Ȳ��ƽ��ֵΪ________�森
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com