
A.Al的氧化物的水化物可能具有两性
B.At2为有色固体,HAt不稳定,AgAt感光性很强,既不溶于水也不溶于稀酸
C.HClO的酸性一定比H2SO4强
D.H2Se是无色、有毒、比H2S稳定的气体
解析:Al的氧化物的水化物为Al(OH)3,Al(OH)3既能与酸反应又能与碱反应,故具有两性,A选项正确。At为卤素中的最后一种元素,从卤素性质递变规律来看,其单质的熔点,按F2、Cl2、Br2、I2、At2逐渐升高。其中I2为固体,故At2亦为固体。由于元素的非金属性从F到At逐渐减弱,故气态氢化物的稳定性从HF到HAt逐渐减弱,HI不稳定,HAt更不稳定。卤化银的感光性从AgF至AgAt逐渐加强,故AgAt具有很强的感光性,在卤化银中除AgF外,其余都既不溶于水也不溶于稀酸,所以B选项正确。Cl的非金属性比S强,非金属性越强,其最高价氧化物对应的水化物的酸性越强,而HClO中的Cl为+1价,不是Cl的最高价(+7价)氧化物对应的水化物(HClO4),故不能说HClO的酸性一定比H2SO4强。实质上HClO为弱酸,H2SO4为强酸,所以C选项说法错误。Se为34号元素,其电子层排布为 ;S为16号元素,其电子层排布为
;S为16号元素,其电子层排布为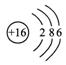 ;Se与S最外层电子数相同,但电子层数Se比S多一个电子层,原子半径Se>S,非金属性Se弱于S,故此H2Se的稳定性比H2S弱,所以D选项说法错误。
;Se与S最外层电子数相同,但电子层数Se比S多一个电子层,原子半径Se>S,非金属性Se弱于S,故此H2Se的稳定性比H2S弱,所以D选项说法错误。
答案:CD


科目:高中化学 来源: 题型:
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | |
| X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:全优设计必修二化学人教版 人教版 题型:021
|
结合元素周期律的知识分析下列说法,其中错误的是 | |
A. |
Al的氧化物的水化物可能具有两性 |
B. |
At2为有色固体,HAt不稳定,AgAt感光性很强,既不溶于水也不溶于稀酸 |
C. |
HClO的酸性一定比H2SO4强 |
D. |
H2Se是无色、有毒、比H2S稳定的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
结合元素周期律的知识分析下列说法,其中错误的是( )
A.Al的氧化物的水化物可能具有两性
B.At2为有色固体,HAt不稳定,AgAt感光性很强,既不溶于水也不溶于稀酸
C.HClO的酸性一定比H2SO4强
D.H2Se是无色、有毒、比H2S稳定的气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com