
| A. | 强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强 | |
| B. | 影响化学平衡常数的因素是温度 | |
| C. | 放热反应不一定能自发进行,而吸热反应也可能自发进行 | |
| D. | 熵增大的反应其焓变一定增大,焓变增大的反应其熵不一定增大 |
分析 A.溶液导电能力取决于溶液中离子浓度的大小,与电解质强弱无关;
B.化学平衡常数只与温度有关;
C.反应是否自发进行的判断依据是△H-T△S<0;
D.熵变是体系混乱度的量度,熵值大,体系混乱度大,焓变为反应的热效应.
解答 解:A.溶液导电能力取决于溶液中离子浓度的大小,与离子浓度成正比,与电解质强弱无关,如果弱电解质溶液中离子浓度大于强电解质溶液,则弱电解质溶液导电能力大于强电解质,所以强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强,故A正确;
B.化学平衡常数是温度的函数,只随温度的变化而变化,则影响化学平衡常数的因素是温度,故B正确;
C.反应的自发性由焓变和熵变共同决定,即自由能决定,△G=△H-T△S,△G为自由能变化,△H为焓变,T为热力学温度,△S熵变.当△G<0时反应能自发进行,△G>0时反应不能自发进行,焓变小于零的反应,△H<0,若△S<0,高温下可以△G>0,反应不能自发进行,熵变大于零的反应,△S>0,若△H>0,高温下可以△G<0时反应可自发进行,故C正确;
D.熵变是体系混乱度的量度,熵值大,体系混乱度大,焓变为反应的热效应,二者没有必然联系,故D错误.
故选D.
点评 本题考查了溶液的导电性、化学平衡常数的影响因素、反应热、自由能判据,题目难度较小,注意反应的自发性由焓变和熵变共同决定.


科目:高中化学 来源: 题型:选择题
| A. | Na投入到水中:Na+H2O═Na++OH-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | Al2O3和NaOH溶液:Al2O3+2OH-═2AlO2-+H2O | |
| D. | FeCl2溶液跟Cl2反应:Fe2++Cl2═Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用澄清石灰水鉴别SO2和CO2 | |
| B. | 用KSCN溶液鉴别FeCl2和FeCl3溶液 | |
| C. | 用焰色反应鉴别NaCl溶液和KCl溶液 | |
| D. | 用过量的NaOH溶液鉴别AlCl3溶液和MgCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | 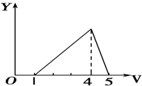 | C. | 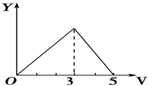 | D. | 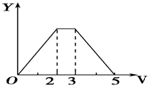 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 单位时间内生成n molO2的同时生成2n molNO | |
| B. | 混合气体的平均相对分子质量不再改变 | |
| C. | 混合气体的颜色不再改变 | |
| D. | 混合气体的密度不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海南岛四面环海,水资源丰富,不必节约用水 | |
| B. | 水体富营养化是因为水体中植物营养物质过多蓄积而引起的污染 | |
| C. | 可通过长期饮用含Ca2+浓度较高的水来补钙 | |
| D. | 长期饮用纯净水更科学 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com