
·ÖĪö £Ø1£©¾Żn=cv¼ĘĖć£»
£Ø2£©øł¾ŻBaŌ×ÓŹŲŗć¼“n£ØBa£ØOH£©2£©=n£ØBaSO4£©£¬²¢øł¾ŻĘäÖŠBaSO4µÄĮæĒóBa£ØOH£©2£»
£Ø3£©øł¾ŻĮņŌŖĖŲŹŲŗć¼“n£ØH2SO4£©=n£ØBaSO4£©£¬²¢øł¾ŻĒāŌŖĖŲŹŲŗćn£ØHCl£©+2n£ØH2SO4£©=n£ØH+£©£¬ĒóHClµÄĪļÖŹµÄĮæÅØ¶Č£»
½ā“š ½ā£ŗ£Ø1£©n£ØH+£©=cv=2.5mol•L-1”Į0.2L=0.5mol
¹Ź“š°øĪŖ£ŗ0.5
£Ø2£©n£ØBaSO4£©=$\frac{m£ØBaS{O}_{4}£©}{M}$=$\frac{4.66}{233}$=0.02mol
øł¾ŻBaŌ×ÓŹŲŗć¼“n£ØBa£ØOH£©2£©=n£ØBaSO4£©=0.02mol
C£ØBa£ØOH£©2£©=$\frac{n£ØBa£ØOH£©_{2}£©}{V}$=$\frac{0.02}{0.2}$=0.1mol•L-1
¹Ź“š°øĪŖ£ŗ0.1
£Ø3£©øł¾ŻĮņŌŖĖŲŹŲŗć¼“n£ØH2SO4£©=n£ØBaSO4£©=0.02mol
øł¾ŻĒāŌŖĖŲŹŲŗćn£ØHCl£©+2n£ØH2SO4£©=n£ØH+£©£¬¼“n£ØHCl£©+2”Į0.02=0.5£¬½āµĆn£ØHCl£©=0.46mol
c£ØHCl£©=$\frac{0.46mol}{0.2L}$=2.3mol•L-1
¹Ź“š°øĪŖ£ŗ2.3
µćĘĄ ±¾Ģāæ¼²éøł¾Ż·½³ĢŹ½½ųŠŠµÄÓŠ¹Ų¼ĘĖć£¬ÄѶČÖŠµČ£¬×¢ŅāĮņĖįøłĒ”ŗĆĶźČ«³ĮµķŹ±£¬ČÜŅŗĪŖĖįŠŌ£¬Ļąµ±ÓŚHClĪ“·“Ó¦£¬×¢Ņāøł¾ŻŹŲŗć½ųŠŠµÄ¼ĘĖć£¬æÉŅŌ¼ņ»Æ¼ĘĖć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
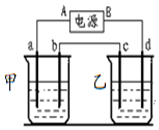 °“ČēĶ¼µÄŹµŃé×°ÖĆ½ųŠŠŹµŃ飬ĘäÖŠa”¢b”¢c”¢d¾łĪŖ¶čŠŌµē¼«£®µē½āÖŹČÜŅŗ·Ö±šĪŖĮņĖįĶŗĶ±„ŗĶĀČ»ÆÄĘČÜŅŗ£¬ĶصēŅ»¶ĪŹ±¼äŗó£¬øł¾ŻĻĀĮŠĻÖĻó×÷³öÅŠ¶Ļ£ŗ”¾¼ŁÉčµē½āÖŹ¾ł×ćĮæ”æ
°“ČēĶ¼µÄŹµŃé×°ÖĆ½ųŠŠŹµŃ飬ĘäÖŠa”¢b”¢c”¢d¾łĪŖ¶čŠŌµē¼«£®µē½āÖŹČÜŅŗ·Ö±šĪŖĮņĖįĶŗĶ±„ŗĶĀČ»ÆÄĘČÜŅŗ£¬ĶصēŅ»¶ĪŹ±¼äŗó£¬øł¾ŻĻĀĮŠĻÖĻó×÷³öÅŠ¶Ļ£ŗ”¾¼ŁÉčµē½āÖŹ¾ł×ćĮæ”æ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | pHŹŌÖ½Ź¹ÓĆÖ®Ē°ŠčÓĆÕōĮóĖ®ČóŹŖ | |
| B£® | ÓĆ¹ć·ŗpHŹŌÖ½²ā¶ØijČÜŅŗµÄpHĪŖ3.5 | |
| C£® | pH=7µÄČÜŅŗŅ»¶Ø³ŹÖŠŠŌ | |
| D£® | ÖŠŠŌČÜŅŗµÄc£ØH+£©=$\sqrt{K_W}$mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ÖŅŗ”¢ŻĶČ””¢ÕōĮó | B£® | ŻĶČ””¢ÕōĮ󔢷ÖŅŗ | C£® | ·ÖŅŗ”¢ÕōĮó”¢ŻĶČ” | D£® | ÕōĮó”¢ŻĶČ””¢·ÖŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ĪļÖŹ | ČŪµć/”ę | ·Šµć/”ę | ĘäĖüŠŌÖŹ |
| SO2Cl2 | -54.1 | 69.1 | ¢ŁŅ×Ė®½ā²śÉś“óĮæ°×Īķ ¢ŚŅ×·Ö½ā£ŗSO2Cl2$\frac{\underline{\;”÷\;}}{\;}$SO2”ü+Cl2”ü |
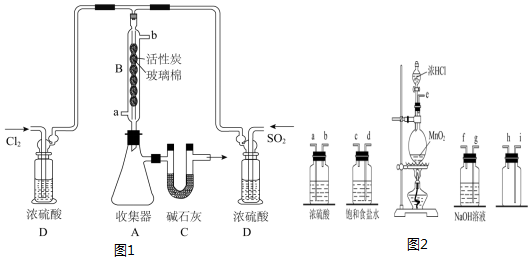
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ²Ł ×÷ | ČÜŅŗÅØ¶Č |
| ķĄĀė·ÅŌŚ×óÅĢ”¢NaOH¹ĢĢå·ÅÓŅÅĢ½ųŠŠ³ĘĮæ£Ø1gŅŌĻĀŹ¹ÓĆÓĪĀė£© | ¢Ł |
| ×ŖŅĘČÜŅŗŹ±ÓŠÉŁĮæŅŗĢåČ÷Āäµ½ČŻĘ÷Ķā | ¢Ś |
| ¶ØČŻŹ±ø©ŹÓæĢ¶ČĻß | ¢Ū |
| Ņ”ŌČŗó¹Ū²ģµ½ŅŗĆęµĶÓŚæĢ¶ČĻߣ¬Į¢¼“²¹³äĖ®µ½°¼ŅŗĆęÓėæĢ¶ČĻßĖ®Ę½ĻąĒŠ | ¢Ü |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com