
 我校环保兴趣小组在处理污水样品时,需用质量分数为37%的浓盐酸(密度为1,.19g/cm3)配制成250mL 0.1mol•L-1的盐酸溶液.
我校环保兴趣小组在处理污水样品时,需用质量分数为37%的浓盐酸(密度为1,.19g/cm3)配制成250mL 0.1mol•L-1的盐酸溶液.分析 (1)根据配制一定物质的量浓度的溶液使用的仪器分析需要的仪器和缺少的仪器;再根据玻璃棒在操作中的作用解答;
(2)根据c=$\frac{1000ρω}{M}$计算出需要浓盐酸的浓度,再根据配制250mL 0.1mol•L-1的盐酸溶液需要的氯化氢的物质的量计算出需要的体积;配制250mL溶液需要250mL容量瓶;
(3)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶来对操作顺序进行排序;
(4)根据容量瓶的正确使用方法进行判断;
(5)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
解答 解:(1)分液漏斗用来萃取和分液,配制一定物质的量浓度溶液不用分液漏斗,故选C;还缺少玻璃棒,在浓盐酸稀释时用玻璃棒搅拌,转移液体时用玻璃棒引流,
故答案为:C;玻璃棒;搅拌;引流;
(2)质量分数为37%的浓盐酸(密度为1.19g/cm3)的物质的量浓度为:c=$\frac{1000ρω}{M}$=$\frac{1000×1.19×37%}{36.5}$=12.1(mol/L),所需浓盐酸体积V=$\frac{0.1mol/L×0.25L}{12.1mol/L}$=0.0021L=2.1mL,故选择10mL量筒,故答案为:A;
(3)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序是③①④②,故答案为:③①④②;
(4)A、容量瓶使用时,应先检查是否漏水,然后用蒸馏水洗涤干净即可,故A正确;
B、容量瓶洗净后不能用所配制溶液润洗,否则影响配制的溶液的浓度,故B错误;
C、容量瓶只能用来配制溶液,不能在容量瓶中溶解,应该在烧杯中溶解,故C错误;
D、容量瓶只能用来配制溶液,不能在容量瓶中稀释,应该在烧杯中稀释,故D错误;
E、摇匀时,盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转,故E正确;
故选AE;
(5)①容量瓶中有少量蒸馏水,对所配溶液的浓度无影响,故答案为:无影响;
②烧杯和玻棒没有洗涤2-3次,则会导致溶质的损失,则浓度偏低,故答案为:偏低;
③稀释浓HCl时,没有冷却就立即转移到容量瓶中,则冷却后溶液体积偏小,浓度偏高,故答案为:偏高;
④配制的溶液装入洁净的但有少量蒸馏水的试剂瓶中,则溶液被稀释,浓度偏小,故答案为:偏低;
⑤若定容时俯视,所配溶液的体积偏小,则物质的量浓度偏高,故答案为:偏高.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | G→a→c→f→b→d→c→b | B. | G→c→b→d→c→f→c→a | C. | G→a→e→f→b→d→c | D. | G→b→f→a→d→c→b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若硫酸足量会有氢气生成 | |
| B. | 离子方程式为Cu2O+2H+=Cu2++Cu+H2O | |
| C. | 会得到蓝色溶液 | |
| D. | 氧化剂、还原剂均是Cu2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑧ | B. | ①②③⑤ | C. | ②③④⑥ | D. | ②③④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某吸热反应能自发进行,因此该反应一定是熵增反应 | |
| B. | 合成氨的反应达到平衡后,给体系加压(压缩),活化分子百分数增加,所以反应速率加快 | |
| C. | 活化分子之间的碰撞都是有效碰撞,都能引发化学反应 | |
| D. | 增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L | B. | 0.5mol/L | C. | 4mol/L | D. | 1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 转移电子4.8NA个 | B. | 生成气体的体积42.56L(标准状况) | ||
| C. | 还原剂比氧化剂多0.2mol | D. | 被还原的氮原子是11.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
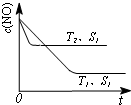 对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题:
对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题: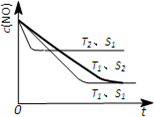 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com