
钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、SiO2等杂质。利用钛铁矿制备二氧化钛,进一步制备钛单质,流程如图:
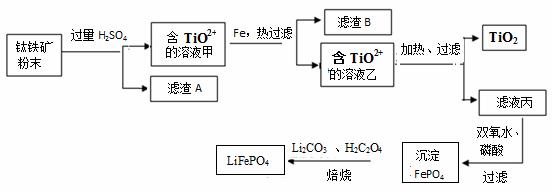
已知:FeTiO3+4H+=Fe2++TiO2++2H2O
草酸(C2H2O4)具有很强还原性,易被氧化成二氧化碳
(1)化合物FeTiO3中铁元素的化合价是 。
(2)钛铁矿加入过量H2SO4后,得到的滤渣A为_______________(填化学式)。
(3)含TiO2+ 溶液乙转化生成TiO2的离子方程式是 。
(4)由滤液丙制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是 。
(5)用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。滴定分析时,称取TiO2(摩尔质量为M g/mol)试样w g,消耗c mol/L NH4Fe(SO4)2标准溶液VmL,则TiO2质量分数为 (用代数式表示)。

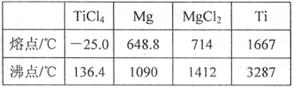 (6)TiO2制取单质Ti,涉及到的步骤如下:
(6)TiO2制取单质Ti,涉及到的步骤如下:
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
反应②的方程式是 , 由TiCl4→Ti需要在Ar气中进行的理由是 。反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据表中信息,需加热的温度略高于 ℃即可。
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
【答案】I.(1)+2 (1分) (2)SiO2 (1分)
(3)TiO2-+H2O TiO2↓+2H+ (2分)
TiO2↓+2H+ (2分)
(4)20:9 (2分)
(5)cVM/1000W 或 cVM/1000W ×100﹪(2分)
(6)TiCl4 +2Mg  2MgCl2 + Ti (2分);防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用(2分) 1412 (2分)
2MgCl2 + Ti (2分);防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用(2分) 1412 (2分)
【命题立意】本题考查学生利用钛铁矿制备二氧化钛的工艺流程理解、阅读题目获取信息能力、氧化还原反应及方程式的书写等,难度中等;
【解析】(1)钛铁矿的主要成分为FeTiO3 ,可表示为FeO·TiO2 ,可知Fe的化合价为+2价;(2)钛铁矿中只有SiO2不与硫酸反应,因此滤渣A的成分是SiO2。(3)TiO2+转化为TiO2,Ti的化合价不变,发生的是TiO2+的水解反应,过滤后未加其他反应物,所以TiO2+与H2O反应,生成TiO2,同时生成H+,反应方程式为:TiO2-+H2O TiO2↓+2H+;(4)分析反应流程,H2O2把Fe2+氧化为Fe3+,H2C2O4把Fe3+还原为Fe2+,H2O2中O由-1价变为-2价,H2C2O4由+3价变为+4价,根据电子转移总数相等得:m(H2O2)×17÷200g/mol×2=m(H2C2O4)÷90g/mol×2,得m(H2O2):m(H2C2O4)= 20/9;(5) 根据得失电子守恒,有:1Ti3+~1Fe3+,故n(Fe3+)=n(Ti3+)=n(TiO2)=cV×10-3mol,其质量分数为为:cVM/1000W 或 cVM/1000W ×100﹪;(6)在800℃条件下,四氯化钛和镁反应生成氯化镁和钛,反应方程式为:TiCl4 +2Mg
TiO2↓+2H+;(4)分析反应流程,H2O2把Fe2+氧化为Fe3+,H2C2O4把Fe3+还原为Fe2+,H2O2中O由-1价变为-2价,H2C2O4由+3价变为+4价,根据电子转移总数相等得:m(H2O2)×17÷200g/mol×2=m(H2C2O4)÷90g/mol×2,得m(H2O2):m(H2C2O4)= 20/9;(5) 根据得失电子守恒,有:1Ti3+~1Fe3+,故n(Fe3+)=n(Ti3+)=n(TiO2)=cV×10-3mol,其质量分数为为:cVM/1000W 或 cVM/1000W ×100﹪;(6)在800℃条件下,四氯化钛和镁反应生成氯化镁和钛,反应方程式为:TiCl4 +2Mg  2MgCl2 + Ti;Mg是活泼金属,能与空气中多种物质反应,因此可得出Ar气作用为保护气, 防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用;由表中数据可知,Mg、MgCl2的沸点最高是1412℃,而Ti的熔点为1667℃,所以当加热的温度略高于1412℃时Mg、MgCl2以气体的形式除去,得到Ti。
2MgCl2 + Ti;Mg是活泼金属,能与空气中多种物质反应,因此可得出Ar气作用为保护气, 防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用;由表中数据可知,Mg、MgCl2的沸点最高是1412℃,而Ti的熔点为1667℃,所以当加热的温度略高于1412℃时Mg、MgCl2以气体的形式除去,得到Ti。


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
一定温度下,10 mL 0.40 mol·L-1 H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)( )
A.0~6 min的平均反应速率:
v(H2O2)≈3.3×10-2 mol·L-1·min-1
B.6~10 min的平均反应速率:
v(H2O2)<3.3×10-2 mol·L-1·min-1
C.反应到6 min时,c(H2O2)=0.30 mol·L-1
D.反应到6 min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
为了证明醋酸是弱电解质,甲、乙、丙、丁四人分别选用下列试剂进行实验:0.1 mol·L-1醋酸溶液、0.1 mol·L-1盐酸、pH=3的盐酸、pH=3的醋酸、CH3COONa晶体、NaCl晶体、CH3COONH4晶体、蒸馏水、锌粒、pH试纸、酚酞、NaOH溶液等。
(1)甲取出10 mL 0.1 mol·L-1的醋酸溶液,用pH试纸测出其pH=a,确定醋酸是弱电解质,则a应该满足的关系是__________________________,
理由是________________________________________________________________________。
(2)乙分别取pH=3的醋酸和盐酸各1 mL,分别用蒸馏水稀释到100 mL,然后用pH试纸分别测定两溶液的pH,则可认定醋酸是弱电解质,判断的依据是________________________________________________________________________。
(3)丙分别取pH=3的盐酸和醋酸各10 mL,然后加入质量相同的锌粒,醋酸放出H2的速率快,则认定醋酸是弱电解质,你认为这一方法正确吗?________,请说明理由:_____________________________。
(4)丁用CH3COONa晶体、NaCl晶体、蒸馏水和酚酞做实验,也论证了醋酸是弱酸的事实,该同学的实验操作和现象是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有pH=2的醋酸甲和pH=2的盐酸乙:
(1)取10 mL的甲溶液,加入等体积的水,醋酸的电离平衡________(填“向左”、“向右”或“不”)移动;若加入少量的冰醋酸,醋酸的电离平衡________(填“向左”、“向右”或“不”)移动,若加入少量无水醋酸钠固体,待固体溶解后,溶液中c(H+)/c(CH3COOH)的值将________(填“增大”、“减小”或“无法确定”)。
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为pH(甲)________(填“大于”、“小于”或“等于”)pH(乙)。若将甲、乙两溶液等体积混合,溶液的pH=__________。
(3)各取25 mL的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和至pH=7,则消耗的NaOH溶液的体积大小关系为V(甲)________(填“大于”、“小于”或“等于”)V(乙)。
(4)取25 mL的甲溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+)、c(CH3COO-)的大小关系为c(Na+)________(填“大于”、“小于”或“等于”)c(CH3COO-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,充电时,总反应为Na2Sx === 2Na + xS(3<x<5),其反应原理如图所示,下列说法错误的是( )
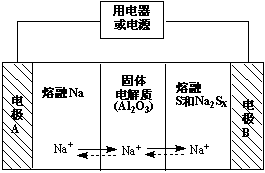
A.放电时,电极A为负极
B.该电池工作的适宜温度应控制10℃左右
C.放电时,内电路中Na+的移动方向为A到B
D.充电时,阳极的电极反应式为 Sx2- - 2e- === xS
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.硫酸钠溶液和醋酸铅溶液均能使蛋白质变性
B.金属腐蚀的本质是金属原子失电子被氧化的过程
C.工业生产玻璃、水泥、陶瓷,均需要用石灰石为原料
D.人造纤维、合成纤维和光导纤维都是有机高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。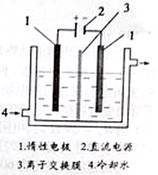 碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如右图所示。
碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如右图所示。
请回答下列问题:
(1)碘是 (填颜色)固体物质,实验室常用 方法来分离提纯含有少量杂质的固体碘。
(2)写出碘酸钾在酸性介质中与过氧化氢反应的离子方程式:
(3)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。图中的序号3应为 离子交换膜(填“阳”或“阴”);电解时,阳极上发生反应的电极反应式为 。
(4)教材中利用KI与空气的反应来探究反应速率与温度的关系,现有1mol/L的KI溶液、0.1mol/L的H2SO4溶液、淀粉溶液,则实验时这几种试剂的加入顺序为:
KI溶液、 、 ;反应的离子方程式为 。
(5)已知KI+I2 KI3,将I2溶于KI溶液,在低温条件下,可制得KI3·H2O。该物质作为食盐加碘剂是否合适?______(填“是”或“否”),并说明理由_______________________________。为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失。下列物质中有可能作为稳定剂的是___________________。
KI3,将I2溶于KI溶液,在低温条件下,可制得KI3·H2O。该物质作为食盐加碘剂是否合适?______(填“是”或“否”),并说明理由_______________________________。为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失。下列物质中有可能作为稳定剂的是___________________。
A.Na2S2O3 B.AlCl3 C.Na2CO3 D.NaNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质的晶体中,化学键类型相同,晶体类型也相同的是( )
A.SO2和SiO2 B.CO2和H2O
C.NaCl和HCl D.CCl4和KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)所有金属纯度越大,越不易被腐蚀( )
(2)纯银器表面变黑和钢铁表面生锈腐蚀原理一样( )
(3)干燥环境下金属不被腐蚀( )
(4)Al、Fe、Cu在潮湿的空气中腐蚀均生成氧化物( )
(5)钢铁发生电化学腐蚀时,负极铁失去电子生成Fe3+( )
(6)在金属表面覆盖保护层,若保护层破损后,就完全失去了对金属的保护作用( )
(7)外加电流的阴极保护法,构成了电解池;牺牲阳极的阴极保护法构成了原电池。二者均能有效地保护金属不容易被腐蚀( )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com