
分析 (1)三价铁离子与硫氰根离子发生络合反应生成血红色硫氰合铁络合物;
(2)KSCN与Fe3+作用使溶液显血红色,与Fe2+作用无此现象,依此进行分析判断.
解答 解:(1)三价铁离子与硫氰根离子发生络合反应生成血红色硫氰合铁络合物,离子方程式为Fe3++3SCN-=Fe(SCN)3,取少量溶液于试管中,加入KSCN溶液,若出现血红色溶液证明原溶液中含Fe3+,
故答案为:取少量溶液于试管中,加入KSCN溶液,若出现血红色溶液证明原溶液中含Fe3+;
(2)KSCN与Fe3+作用使溶液显红色,与Fe2+作用无此现象,故先滴加KSCN溶液,不显血红色,说明原溶液不含有Fe3+;
再加入氯水,溶液显血红色,说明溶液中有Fe3+生成,说明原溶液中含有Fe2+,
故鉴定某溶液中含有Fe2+,最好的方法是:取少量溶液于试管中先加入KSCN溶液无变化,再加氯水溶液变为血红色,证明原溶液中含Fe2+,
故答案为:取少量溶液于试管中先加入KSCN溶液无变化,再加氯水溶液变为血红色,证明原溶液中含Fe2+;
点评 本题考查三价铁离子、二价铁离子的检验和性质应用,难度中等.关键是加氧化剂、KSCN溶液的顺序不能颠倒.


科目:高中化学 来源: 题型:选择题

| A. | 由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的△H<0 | |
| B. | 由图Ⅱ知,各平衡状态在t6时,NH3体积分数最小 | |
| C. | 由图Ⅱ知,t3时采取的措施是降低反应体系温度 | |
| D. | Ⅲ在10L容器、850℃时反应,由图知,到4min时,反应放出5.16kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
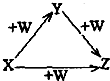
| A. | ①②③ | B. | ①② | C. | ③④ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C4H6 | B. | C2H6 | C. | C6H6 | D. | C4H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水的离子积常数仅表示一定温度下纯水中H+浓度和OH-浓度的乘积 | |
| B. | 水的离子积常数是固定不变的一个数值 | |
| C. | 判断溶液酸碱性的标准是比较H+浓度和OH-浓度的相对大小 | |
| D. | pH=-1的硫酸溶液不存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
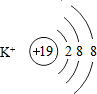 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com