
镀锌铁在发生析氢腐蚀时,若有0.2 mol电子发生转移,下列说法正确的是( )
①有5.6 g金属被腐蚀 ②有6.5 g金属被腐蚀 ③在标准状况下有2.24 L气体放出 ④在标准状况下有1.12 L气体放出
A.①② B.②③
C.①④ D.③④
科目:高中化学 来源: 题型:
向一容积不变的密闭容器中充入一定量A和B,发生如下反应:
xA(g)+2B(s)yC(g) ΔH<0
在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答下列问题:
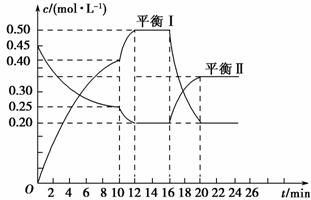
(1)用A的浓度变化表示该反应0~10 min内的平均反应速率v(A)=______________________。
(2)根据图示可确定x∶y=________。
(3)0~10 min容器内压强________(填“变大”、“不变”或“变小”)。
(4)推测第10 min引起曲线变化的反应条件可能是________;第16 min引起曲线变化的反应条件可能是________。
①减压 ②增大A的浓度 ③增大C的量 ④升温 ⑤降温 ⑥加催化剂
(5)若平衡Ⅰ的平衡常数为K1,平衡Ⅱ平衡常数为K2,则K1________K2(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(Ⅰ)21世纪最富有挑战性的课题之一是使汽油氧化直接产生电流。新研制的某汽油燃料电池的工作原理为:一个电极通入空气,另一电极通入汽油蒸气,掺杂了Y2O3 的ZrO2晶体作电解质,它在高温下传导O2-离子,填写下列空白。
(1)汽油燃料电池的能量转化率比汽油在发动机里燃料产生动力的能量转化率________(填“高”或“低”)。
(2)若用丁烷(C4H10)代表汽油,则该燃料电池总反应的化学方程式为__________________________________________________________。
(3)该汽油燃料电池的不足之处是汽油被氧化不完全,产生的________可能堵塞气体通道。
(Ⅱ)古代铁器(埋藏在地下)在严重缺氧的环境中,仍然锈蚀严重(电化学腐蚀)。原因是一种叫做硫酸盐还原菌的细菌,能提供正极反应的催化剂,可将土壤中的SO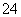 还原为S2-,该反应放出的能量供给细菌生长、繁殖之需。
还原为S2-,该反应放出的能量供给细菌生长、繁殖之需。
(1)写出该电化学腐蚀的正极反应的电极反应式:
_______________________________________________________________。
(2)文物出土前,铁器表面的腐蚀产物可能有(写化学式)
_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
由氢气和氧气反应生成1mol水蒸气,放热241.8 kJ。写出该反应的热化学方程式:_______________________________。
若1 g水蒸气转化成液态水放热2.494 kJ,则反应H2(g)+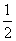 O2(g)===H2O(l)的ΔH=______kJ·mol-1。
O2(g)===H2O(l)的ΔH=______kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
CH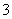 、—CH3、CH
、—CH3、CH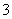 都是重要的有机反应中间体,有关它们的说法正确的是 ( )。
都是重要的有机反应中间体,有关它们的说法正确的是 ( )。
A.它们互为等电子体,碳原子均采取sp2杂化
B.CH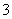 与 NH3、H3O+ 互为等电子体,立体构型均为正四面体形
与 NH3、H3O+ 互为等电子体,立体构型均为正四面体形
C.CH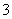 中的碳原子采取 sp2 杂化,所有原子均共面
中的碳原子采取 sp2 杂化,所有原子均共面
D.CH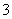 与OH- 形成的化合物中含有离子键
与OH- 形成的化合物中含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如下图所示。
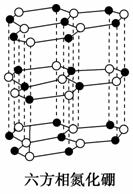
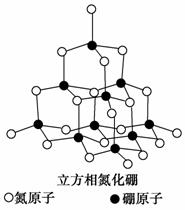
(1)基态硼原子的电子排布式为_________________________________。
(2)关于这两种晶体的说法,正确的是________(填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键
d.两种晶体均为分子晶体
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为________________,其结构与石墨相似却不导电,原因是_________________
_________________________________________________________。
(4)立方相氮化硼晶体中,硼原子的杂化轨道类型为________。该晶体的天然矿物在青藏高原地下约300 km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是 __________。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4含有________ mol配位键。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com