
【题目】下表是元素周期表的一部分,用化学用语回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
4 |
(1)画出元素⑨阴离子的结构示意图:______,⑧正下方的元素原子序数为____
(2)③⑤⑧的原子半径由小到大的顺序为________(填元素符号)。
(3)⑤和⑦的最高价氧化物对应水化物的碱性强弱为___________(填化学式)。
(4)③⑤两种元素的原子按1∶1组成的常见化合物的电子式为____________________。
(5)用电子式表示⑥和⑨形成的化合物的过程:____________________________________。
【答案】![]() 34 O<S<Na NaOH>Al(OH)3
34 O<S<Na NaOH>Al(OH)3 ![]()
![]()
【解析】
根据元素在周期表中的位置,①为H,②为N,③为O,④为F,⑤为Na,⑥为Mg,⑦为Al,⑧为S,⑨为Cl,⑩为Ar。
(1) Cl-阴离子的结构示意图为![]() ,答案为:
,答案为:![]() ;
;
(2) ⑧为S,其正下方的元素为34号元素Se,答案为:34;
(3) ③为O,⑤为Na,⑧为S,原子半径从上到下依次增大,从左到右依次减小,③⑤⑧的原子半径由小到大的顺序为O<S<Na,答案为:O<S<Na;
(4) Na的金属性大于Al,金属性越强,最高价氧化物对应水化物的碱性越强,答案为:NaOH>Al(OH)3;
(5)Na和O按1∶1组成的常见化合物为Na2O2,为离子化合物,其电子式为:![]() ;
;
(6) 用电子式表示MgCl2形成的化合物的过程,即由Cl和Mg原子通过得失电子,形成MgCl2这个离子化合物,答案为:![]() 。
。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】利用天然气可制得以H2、CO等为主要组成的工业原料合成气,反应为CH4(g)+H2O(g)![]() CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)甲烷与水蒸气反应,被氧化的元素是____________(元素符号作答),当生成标准状况下35.84 L合成气时转移电子的物质的量是________。
(2)将2 mol CH4和5 mol H2O(g)通入容积为10 L的反应室,CH4的平衡转化率与温度、压强的关系如图所示。

①若达到A点所需的时间为5 min,则v(H2)=____________________。
②图中的p1______p2(填“<”“>”或“=”),A、B、C三点的平衡常数KA、KB、KC的大小关系是_______。
(3)合成气用于合成氨气时需除去CO,发生反应CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0,下列措施中能使
CO2(g)+H2(g) ΔH<0,下列措施中能使![]() 增大的是________(选填编号)。
增大的是________(选填编号)。
A.降低温度 B.恒温恒容下充入He(g)
C.将H2从体系中分离 D.再通入一定量的水蒸气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下:

(1)浸锰过程中Fe2O3与SO2反应的化学方程式为Fe2O3+ SO2+2H+=2Fe2++ SO42-+ H2O,该反应是经历以下两步反应实现的。写出ⅱ的离子方程式:_____________。
ⅰ:Fe2O3 + 6H+ = 2Fe3++3H2O
ⅱ:……
(2)过滤Ⅰ所得滤液中主要存在的两种金属阳离子为_____________(填离子符号)。
(3)写出氧化过程中MnO2与SO2反应的化学方程式:_________________。
(4)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是_________;向过滤Ⅱ所得的滤液中加入NH4HCO3溶液时温度不宜太高的原因是___________________。

(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有气体生成,写出反应的离子方程式:___________________。
(6)生成的MnCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锥形瓶内盛有气体X,滴管内盛有液体Y。若挤压胶头滴管,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起。气体X和液体Y不可能是( )

A.X是NH3,Y是水
B.X是SO2,Y是NaOH浓溶液
C.X是CO2,Y是稀硫酸
D.X是HCl,Y是NaNO3稀溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个容积为2 L的密闭容器中,加入0.8 mol的A2气体和0.6 mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)![]() 2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是

A. 图中a点的值为0.15 B. 该反应的平衡常数K=0.03
C. 温度升高,平衡常数K值减小 D. 平衡时A2的转化率为62.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用所学化学知识,分析并回答下列各小题。

(1)下列物质属于图1所示化学概念交叉部分的有______(填标号)。
a.氨气 b.硝酸 c.乙醇 d.醋酸钠
(2)下列各反应属于图2中阴影部分所示关系的有_______(填标号)。
a.氨气与浓硝酸
b.氢气与氧气
c.氯气与氯化亚铁溶液
d.铜与氯化铁溶液
(3)下列有关说法正确的是_____(填标号)。
a.核电站把核能转化为电能
b.常温下铜与浓硫酸发生钝化。反应很快停止
c.海水中提取化学物质均涉及到氧化还原反应
d.电解法得到某元素单质,则该元素可能被还原,也可能被氧化
(4)下列各实验过程中,需要检查所用某些仪器是否漏水的有_______(填标号)。
a.氢气还原氧化铜
b.水与煤油混合物分离
c.氯化钠溶液与泥沙分离
d.配制100mL 10mol·L-1碳酸钠溶液
(5)下列关于试剂保存的叙述正确的是_________(填标号)。
a.氢氟酸保存在玻璃瓶中
b.KOH溶液保存在带玻璃塞的细口瓶中
c.溴水保存在带橡胶塞的棕色瓶中
d.KMnO4与乙醇不能放在同一药品厨中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示。下列说法错误是

A. Q位于第三周期IA族
B. X、Y、Z三种元素组成的化合物可能是盐或碱
C. 简单离子半径:M->Q+>R2+
D. Z与M的最高价氧化物对应水化物均为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从牛至精油中提取的三种活性成分的结构简式如下图所示,下列说法正确的是
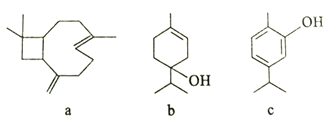
A. a中含有2个手性碳原子(手性碳原子指连有四个不同基团的碳原子)
B. b分子存在属于芳香族化合物的同分异构体
C. c分子中所有碳原子可能处于同一平面
D. a、b、c均能发生加成反应、取代反应、加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1mol/L盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示,下列判断正确的是( )

A. a点时溶液中存在c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B. 0~a段溶液中水电离出的OH-浓度先增大后减小
C. a=0.2
D. ab段发生反应的离子方程式为CO32-+2H+=H2O+CO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com