
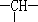 和一个-Cl,它可能的结构有
和一个-Cl,它可能的结构有| 15.0g |
| 100g/mol |
| 2.7g |
| 18g/mol |
| 1.68L |
| 22.4L/mol |
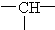 和 一个-Cl,两个甲基和一个氯原子只能位于边上,两个亚甲基只能连接两个原子或原子团,一个次亚甲基连接3个原子或原子团,根据各个基团连接的原子或原子团个数判断其结构.
和 一个-Cl,两个甲基和一个氯原子只能位于边上,两个亚甲基只能连接两个原子或原子团,一个次亚甲基连接3个原子或原子团,根据各个基团连接的原子或原子团个数判断其结构.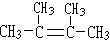 ,名称为2,3-二甲基-2-丁烯;取少量该物质与氢气加成所得产物为2,3-二甲基-丁烷,结构对称,只有2种位置的H,则核磁共振氢谱图上应该出现2个峰,其面积比为12:2=6:1,
,名称为2,3-二甲基-2-丁烯;取少量该物质与氢气加成所得产物为2,3-二甲基-丁烷,结构对称,只有2种位置的H,则核磁共振氢谱图上应该出现2个峰,其面积比为12:2=6:1,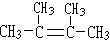 ;2,3-二甲基-2-丁烯;2;6:1;
;2,3-二甲基-2-丁烯;2;6:1;| 15.0g |
| 100g/mol |
| 2.7g |
| 18g/mol |
| 1.68L |
| 22.4L/mol |
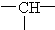 和 一个-Cl,两个甲基和一个氯原子只能位于边上,两个亚甲基只能连接两个原子或原子团,一个次亚甲基连接3个原子或原子团,则符合条件的结构简式为
和 一个-Cl,两个甲基和一个氯原子只能位于边上,两个亚甲基只能连接两个原子或原子团,一个次亚甲基连接3个原子或原子团,则符合条件的结构简式为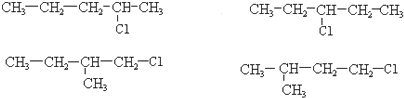 ,共有4种,故答案为:4.
,共有4种,故答案为:4.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
| A、溴水 |
| B、KMn04溶液 |
| C、Na2S04溶液 |
| D、溴的四氯化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③⑤⑦ | B、①②③⑥ |
| C、②③④⑥ | D、①③④⑤⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com