
| A. | 在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2:I-、Br-、Fe2+ | |
| B. | 在含等物质的量的Fe3+、Cu2+、H+的溶液中加入Zn:Fe3+、Cu2+、Fe2+、H+ | |
| C. | 在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2:Ba(OH)2、KOH、K2CO3、BaCO3 | |
| D. | 含等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加入盐酸:AlO2-、Al(OH)3、OH-、CO32- |
分析 A.根据离子的还原性顺序:I->Fe2+>Br-来回答;
B.依据离子的氧化性顺序是:Fe3+>Cu2+>H+>Fe2+来回答;
C.化学反应优先和能生成沉淀的物质间反应;
D.含有AlO2-、OH-、CO32-溶液中,氢离子先是和氢氧根之间发生中和反应.
解答 解:A.在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2,氯气具有氧化性,先和还原性强的离子反应,离子的还原性顺序:I->Fe2+>Br-,故A错误;
B.在含等物质的量的Fe3+、Cu2+、H+的溶液中加入Zn,金属锌先是和氧化性强的离子之间反应,离子的氧化性顺序是:Fe3+>Cu2+>H+>Fe2+,故B错误;
C.在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2,先是和Ba(OH)2之间反应,其次是氢氧化钾,再是和可溶性碳酸盐反应,最后与难溶性碳酸盐反应,故C正确;
D.在含等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加入盐酸,氢离子先是和氢氧根之间发生中和反应,故D错误;
故选:C.
点评 本题考查学生化学反应的先后率知识,注意离子的氧化性、还原性顺序是解题关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 若HA 的电离能力大于A-的水解能力,则有c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-) | |
| B. | 若A-的水解能力大于HA 的电离能力,则有c(Na+)>c(HA)>c(A-)>c(OH-)>c(H+) | |
| C. | 无论该溶液呈酸性还是碱性,都有 c(Na+)+c(H+)=c(A-)+c(OH-) | |
| D. | 无论该溶液呈酸性还是碱性,都有2c(Na+)=c(A-)+c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
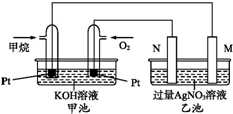 如图是一个甲烷燃料电池工作时的示意图.M、N两电极的质量相同,其中一个为银电极一个为铁电极.
如图是一个甲烷燃料电池工作时的示意图.M、N两电极的质量相同,其中一个为银电极一个为铁电极.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
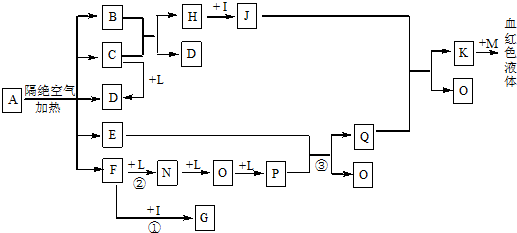
| 物质 | 外观 | 在空气中加热时的现象 | 产物水溶液的酸碱性 |
| X | 黑色粉未 | 燃烧时呈炽红色并发出火花,放出无色气体G | 微弱酸性 |
| Y | 淡黄色晶体 | 首先熔化,然后燃烧,火焰为浅蓝色,放出有刺激性气味的气体 | 弱酸性 |
| Z | 银白色固体 | 燃烧,产生黄色火焰,生成浅黄色固体F | 强碱性 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
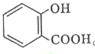 的名称为:2-羟基苯甲酸;在核磁共振氢谱中会出现6组峰;写出其与KHCO3溶液反应的化学方程式:
的名称为:2-羟基苯甲酸;在核磁共振氢谱中会出现6组峰;写出其与KHCO3溶液反应的化学方程式: +KHCO3→
+KHCO3→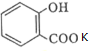 +CO2↑+H2O.
+CO2↑+H2O.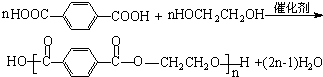 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.01×105Pa,20℃时48g O3含有的原子数为3NA | |
| B. | 1molNa2O2晶体中阴离子数为2 NA | |
| C. | 标准状况下,相同体积的O2、HCl、H2O含有的分子数相同 | |
| D. | 等质量钠,在足量氧气中加热充分反应比在足量氧气(常温)中充分反应失去的电子多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,0.1NA个水分子所占的体积约是2.24 L | |
| B. | 常温常压下,11.2 L CO2中含有11NA个电子 | |
| C. | CH4的摩尔质量和NA个甲烷分子的质量相等 | |
| D. | 常温下,64gSO2气体中含有的原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2(CO):点燃 | |
| B. | 硝酸钾(氯化钠):浓溶液降温结晶 | |
| C. | MgSO4(MgCl2):蒸干、灼烧 | |
| D. | 乙酸(乙醛):加新制氢氧化铜浊液加热,过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com