
| A、强电解质在水中溶解度一定大于弱电解质 |
| B、让一束光线通过蛋白质溶液,会产生丁达尔现现象 |
| C、75mL 2mol/L氯化铵溶液的c(Cl-)与50mL 1 mol/L氯化锅溶液中的c(Cl-)相等 |
| D、浓度为1mol/L的醋酸溶液lL,欲使其浓度变为2mol/L,将溶液加热蒸发浓缩至0.5L |


科目:高中化学 来源: 题型:
| 充电 |
| 放电 |
| A、Cd |
| B、NiO(OH) |
| C、Cd(OH)2 |
| D、Ni(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、光化学烟雾的产生与汽车排放的尾气有关 |
| B、人们用电动自行车代替摩托车是“低碳消费”的行为 |
| C、酸雨是指PH小于7的酸性降水,主要是由煤的燃烧所致的 |
| D、用Cu、O2与稀H2SO4反应代替Cu与浓H2SO4反应制胆矾是“绿色化学”的体现 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下将铁片分别放在浓硝酸和稀硝酸中 | 在浓硝酸中无明显变化,稀硝酸中有气泡 | 稀硝酸的氧化性比浓硝酸强 |
| B | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
| C | 将水蒸气通过灼热的铁粉 | 铁粉变成红棕色粉末 | 铁与水在高温下发生反应 |
| D | 常温下将Al片放入浓硫酸中 | 无明显变化 | Al与浓硫酸不反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③②⑤⑥④ |
| B、③②④①⑦ |
| C、③②④⑤⑦ |
| D、②④①⑦⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 设反应①Fe(s)+CO2(g)?FeO(s)+CO(g)的平衡常数为K1.
设反应①Fe(s)+CO2(g)?FeO(s)+CO(g)的平衡常数为K1.| T(K) | K1 | K2 |
| 973 | 1.47 | 2.36 |
| 1173 | 2.15 | 1.67 |
查看答案和解析>>
科目:高中化学 来源: 题型:
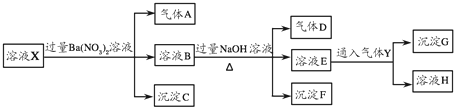
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com