
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
| ||
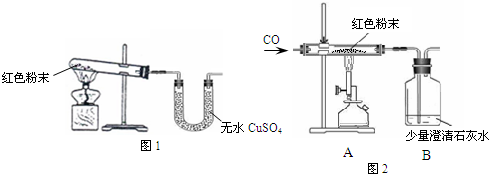
| 反应前 | 反应后 | |
| Ⅰ 组 |
玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
| Ⅱ 组 |
洗气瓶和所盛溶液 的总质量为180.0g |
洗气瓶和瓶中物质 的总质量为183.1g |
查看答案和解析>>
科目:高中化学 来源:2014届河南省许昌平顶山新乡三市高三第一次调研理综化学试卷(解析版) 题型:实验题
测定有机物中碳和氢等元素的含量,最常用的方法是燃烧分析法。即把已知量的样品置于氧气流中,用氧化铜作催化剂,在760℃左右,样品全部被氧化为二氧化碳和水。实验装置如下图所示:
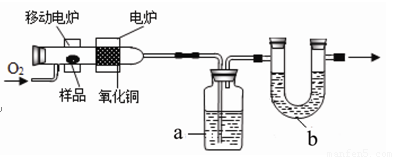
(1)实验时,装置a、b中通常装入的物质分别是 、 。
(2)开始加热之前,要通一段时间的氧气,目的是 ;停止加热后,也要通一段时间的氧气,目的是 。
(3)某次实验中,取用样品烃的含氧衍生物A的质量为2.3g,经测定a装置增重2.7g,b装置增重4.4g。请推算出A物质的实验式: (要求写出计算过程)
(4)经进一步测定得知A的相对分子质量为46,则A的分子式为 。
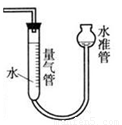
(5)实验发现A物质遇金属钠可以放出氢气,则A物质中具有的官能团为 。同样取2.3g的A,与足量的钠反应,用如图所示装置量取放出的氢气。量取气体时操作水准管的注意事项为 。将量取的气体换算成标准状况体积为cmL,则一个A分子中有 个氢原子被置换了(用含c的表达式表示)。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖北省七市(州)高三4月联考模拟试卷理综化学试卷(解析版) 题型:填空题
Na、Fe、Cu、Al是常见的金属元素,请按要求回答下列问题:
(1)一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为______。
(2)向氯化铜溶液中加入一定量的铁粉和铝粉混合物,充分反应后,下列情况可能出现的是______ (填编号)。
a.溶液中有Cu2+、Fe2+、Al3+,不溶物为Cu b.溶液中有Fe2+、Al3+,不溶物为Cu、Fe
c.溶液中有Fe3+、Al3+,不溶物为Cu d.溶液中有Fe2+,不溶物为Cu、Al
(3)将一定质量的铁、铝、铜合金,加入lL一定物质的量浓度的硝酸中,合金完全溶解,测得溶液中(忽略溶液体积的变化)c(H+)=0.5mol/L、c(Cu2+)=0.3mol/L、c(Al3+)=0.2mol/L、c(NO3-)=2mol/L,则混合物中铁的质量为______。
(4)铁的某种氧化物的化学式表示为FexO(x<1),已知铁元素在该氧化物中的质量分数为75%,则x=______ (精确至0.01)。
(5)Na-AI/FeS是一种可充电电池,电池中用含Na+导电固体作为电解质,在工作过程中Na+的物质的量保持不变。
①若该正极的电极反应式表示为:2Na++FeS+2e-=Na2S+Fe,则电池的负极反应式可表示为_____;充电时,阳极发生反应的物质是______。
②用该电池作电源,组成如图所示装置,若通电5min时,铜电极质量增加1.08 g,则该电源电极X名称为______。图中装置A、C的pH变化为:A ______、C ______ (填“增大” “减小”或“不变”)。

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
为测定镁铝合金(不含其它元素)中铝的质量分数,甲乙两个学习小组设计了下列二种不同的实验方案进行探究。请回答下列问题:
(一)甲组:
实验方案:镁铝合金![]() 测定剩余固体质量
测定剩余固体质量
实验步骤:
①称量 用托盘天平称量2.7g镁铝合金粉末
②溶解 把①中药品加入烧杯中,用规格为 mL的量筒量取一定体积1mol/L NaOH 溶液加入烧杯中,不断搅拌,充分反应
③过滤
④洗涤 若未对过滤所得固体进行洗涤,测得铝的质量分数将 (填“偏高”、“偏低”或“不变” ),证明固体已洗涤干净的方法为
⑤干燥、称量剩余固体
(二)乙组:
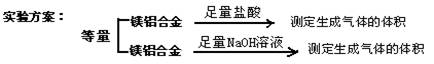
实验装置:
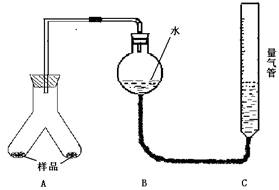
实验步骤:
①图连接好装置
②称取两份质量均为0.3g 的镁铝合金样品粉末,分别放入A装置左右两个管中,向B装置中加入一定量的水,把装置A、B的胶塞塞好,然后调节C的高度使B和C中的液面相平,记录下此时的体积为112 mL
③通过注射器的针头向装置A左侧管中注入足量的稀盐酸,等不再有气泡产生时,调节装置C的高度,使B和C中的液面相平时记录下此时的体积为448mL
④通过另一针头向装置A右侧管中加入足量的稀NaOH溶液,等不再有气泡产生时,调节装置C的高度,使B和C中的液面相平时记录下此时的体积为672mL。
问题和讨论:
(1)上述实验步骤①和②之间必须加一步 的操作,具体方法为 。
(2)为使气体体积测定结果不至于引起很大偏差,除了应注意使B和C中的液面相平外,在反应完全后至读数之前,还需要注意的关键问题是(只需写出1点) 。
(3)计算合金中铝的质量分数时,是否需要将气体体积折算为标准状况的体积 。
查看答案和解析>>
科目:高中化学 来源: 题型:
植物生长需要营养,实验室现有一包由氯化铵和硫酸铵混合而成的白色粉末,课外小组的同学按下图实验设计进行实验,测定这种混合物中各组分的含量,以便给植物施用。
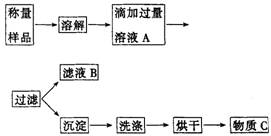
(1)溶液A中溶质的化学式________。
(2)他将样品放入托盘天平的右盘中,样品质量记录游码为0.4g,左边的托盘里的砝码为16g,则样品质量是_____g。
(3)若过滤使用的仪器和用品已有:滤纸、铁架台、铁圈、烧杯、漏斗,还需要补充的仪器或用品是________________________。
(4)怎样证明滴加溶液A已经过量,简述操作方法_______________________________________________。
(5)若物质C的质量为23.3g,那么原混合物中氯化铵的质量分数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com