
如图装置电解一段时间,当某极析出0.32gCu时,I、Ⅱ、Ⅲ中溶液pH分别为 (溶液足量,体积均为100mL且电解前后溶液体积变化及气体的溶解忽略不计)()
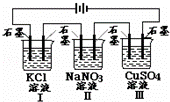
A. 13、7、1 B. 12、7、2 C. 1、7、13 D. 7、13、1
考点: 电解原理.
分析: 由离子放电顺序可知,电解时,I、Ⅱ、Ⅲ中溶液电极方程式分别为2KCl+2H2O 2KOH+H2↑+Cl2↑、2H2O
2KOH+H2↑+Cl2↑、2H2O 2H2↑+O2↑、2CuSO4+2H2O
2H2↑+O2↑、2CuSO4+2H2O 2Cu+O2↑+2H2SO4,由铜的质量计算转移电子的物质的量,进而计算各溶液的pH.
2Cu+O2↑+2H2SO4,由铜的质量计算转移电子的物质的量,进而计算各溶液的pH.
解答: 解:n(Cu)=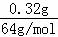 =0.005mol,由电极反应Cu2++2e﹣=Cu可知转移电子为0.01mol,
=0.005mol,由电极反应Cu2++2e﹣=Cu可知转移电子为0.01mol,
电解时,I、Ⅱ、Ⅲ中溶液电极方程式分别为2KCl+2H2O 2KOH+H2↑+Cl2↑、2H2O
2KOH+H2↑+Cl2↑、2H2O 2H2↑+O2↑、2CuSO4+2H2O
2H2↑+O2↑、2CuSO4+2H2O 2Cu+O2↑+2H2SO4,
2Cu+O2↑+2H2SO4,
I中生成0.01molOH﹣,c(OH﹣)=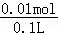 =0.1mol/L,pH=13,
=0.1mol/L,pH=13,
Ⅱ电解水,溶液呈中性,pH=7,
Ⅲ中生成0.01molH+,c(H+)=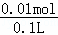 =0.1mol/L,pH=1,
=0.1mol/L,pH=1,
故选A.
点评: 本题考查电解原理,侧重于学生的分析能力和计算能力的考查,为2015届高考高频考点,难度中等,注意把握离子的放电顺序以及电解方程式的书写,为解答该题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
(1)147gH2SO4中含 mol原子,与 g CO2所含有的氧原子数相同.
标准状况下,2.4g某气体的体积为672mL,则此气体的相对分子质量为 .
(3)在标准状况下,V L氨气溶于1L水中,所得溶液的密度为ρg•cm﹣3,溶液的质量分数为ω.则此溶液的物质的量浓度为: 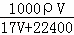 或
或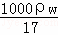 mol/L
mol/L
(4)将Wg胆矾(CuSO4 •5H2O )溶解在VmL水中,得到饱和溶液,测得该饱和溶液的密度为ρg/cm3,则溶液的物质的量浓度为 mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 标准状况下任何气体的摩尔体积都是22.4 L |
|
| B. | 1mol气体的体积若是22.4 L,它必定处于标准状况 |
|
| C. | 两种气体的物质的量之比等于其原子个数比 |
|
| D. | 标准状况下,1mol H2和O2的混合气体的体积是22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)现有1mol/L CaCl2溶液0.5L,Cl﹣的物质的量浓度为 mol/L.
(2)标准状况下,33.6L的HCl所具有的物质的量为 mol,将其溶解于水配成3L的溶液,所得盐酸的物质的量浓度为 mol/L.
(3)8gNaOH溶于 g水中,才能使每10个水分子中溶有一个钠离子.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知S(s)+O2(g)=SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2,△H1和△H2的大小关系为()
A. △H1>△H2 B. △H1<△H2 C. △H1﹦△H2 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是()
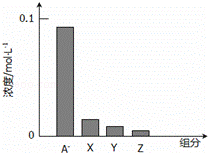
A. HA为强酸
B. 该混合液pH=7
C. 图中X表示HA,Y表示OH﹣,Z表示H+
D. 该混合溶液中:c(A﹣)+c(Y)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度和压强条件下发生了反应:CO2(g)+3H2 (g)⇌CH3OH(g)+H2O(g)△H<0,反应达到平衡时,改变温度(T)和压强(p),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(p)的关系判断正确的是()

A. P3>P2 T3>T2 B. P2>P4 T4>T2
C. P1>P3 T3>T1 D. P1>P4 T2>T3
查看答案和解析>>
科目:高中化学 来源: 题型:
1)在一个容积为3L的密闭容器内进行如下反应:N2(气)+3H2(气)⇌2NH3(气).反应开始时,n(N2)=1.5mol,n(H2)=4.4mol,2min后达到平衡状态,n(H2)=3.5mol.用NH3的浓度变化来表示该反应的反应速率为 ,2min末N2的浓度 ,平衡时N2的转化率为 .
(2)在密闭容器中,对于反应:N2(g)+3H2(g)⇌2NH3(g),在反应起始时N2和H2 分别为5mol和15mol,当达到平衡时,N2的转化率为20%.若以NH3为起始反应物,反应条件与上述反应相同时,欲使其达到平衡时各成分的百分含量与前者相同,则NH3的起始物质的量为 ,NH3的转化率 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com