
| A. | C | B. | P | C. | O | D. | S |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题

| A. | 乙醇不能使酸性高锰酸钾溶液褪色 | |
| B. | 物质B的溶液不能与碳酸钙反应 | |
| C. | CH3COOCH2CH3的同分异构体中能与碳酸氢钠溶液反应的有两种 | |
| D. | 反应④属于取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ③
③ ④
④
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
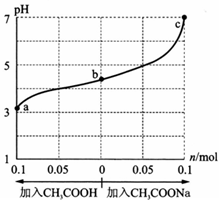 在25℃时,将 1.0L wmoI/L CH3COOH 溶液与 0.1mol NaOH固体混合,充分反应.然后向混合液中加入CH3COOH或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示. 下列叙述正确的是( )
在25℃时,将 1.0L wmoI/L CH3COOH 溶液与 0.1mol NaOH固体混合,充分反应.然后向混合液中加入CH3COOH或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示. 下列叙述正确的是( )| A. | a、b、c对应的混合液中,水的电离程度由大到小的顺序是c>a>b | |
| B. | b点混合液中 c(Na+)>c(CH3COO-) | |
| C. | 加入CH3COOH过程中,$\frac{c(N{a}^{+})•c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$增大 | |
| D. | 25℃时,CH3COOH的电离平衡常数Ka=$\frac{0.2×1{0}^{-7}}{w-0.1}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解CuCl2溶液,阴极析出16g铜时,电极上转移的电子数为NA | |
| B. | 12 g石墨中含有C-C键的个数为1.5NA | |
| C. | 12 g金刚石中含有C-C键的个数为4NA | |
| D. | SiO2晶体中每摩尔硅原子可与氧原子形成2NA个共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,与CO互为等电子体且带1个单位负电荷的阴离子化学式为CN-.
,与CO互为等电子体且带1个单位负电荷的阴离子化学式为CN-.
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
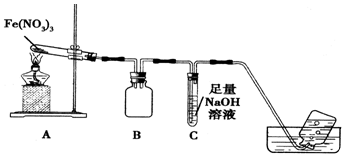
| 试验编号 | 实验操作 | 现象 |
| a | 向10mL 3mol•L-1KNO3酸性溶液(pH=1)中插入一根洁净的银丝,并滴加氯化钠溶液 | 无沉淀生成 |
| b | 向10mL 3mol•L-1AgNO3溶液中滴加2mL 0.1mol•L-1FeSO4溶液,振荡;再滴加酸性高锰酸钾溶液 | 紫红色溶液不褪色 |
| c | 向10mL 3mol•L-1Fe(NO3)3溶液(pH=1)中插入一根洁净的银丝,并滴加氯化钠溶液 | 产生白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com