
| A. | 质子数为53,中子数为78的碘原子:53131I | |
| B. | CH4分子的比例模型: | |
| C. | Na+ 的结构示意图: | |
| D. | NaOH的电离方程式:NaOH?Na++OH- |
分析 A.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
B. 为球棍模型,不是比例模型;
为球棍模型,不是比例模型;
C.钠离子的活动时为11,核外电子总数为10,最外层达到8电子稳定结构;
D.NaOH在溶液中完全电离,电离方程式应该为等号.
解答 解:A.质子数为53,中子数为78的碘原子的质量数=53+78=131,该原子可以表示为:53131I,故A正确;
B.甲烷为正面体结构,由原子相对大小表示空间结构为比例模型,CH4分子正确的比例模型为: ,故B错误;
,故B错误;
C.Na+的核外电子总数为10,其离子结构示意图为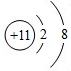 ,故C错误;
,故C错误;
D.NaOH为强电解质,在溶液中完全电离,正确的电离方程式为:NaOH=Na++OH-,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及离子结构示意图、元素符号、比例模型与球棍模型、电离方程式等知识,明确常见化学用语的书写原则为解答关键,试题侧重考查学生的规范答题能力.


 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:NH4+、K+、ClO-、Cl- | |
| B. | 使酚酞变红色的溶液中:Na+、Na+、SO32-、NO3- | |
| C. | 能与金属铝反应生成氢气的溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | 无色透明的溶液中:K+、Cu2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
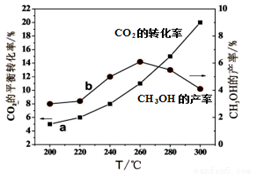 甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:| 温度(℃) | 500 | T |
| CO2的平衡转化率 | 60% | 40% |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
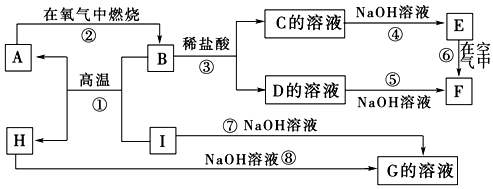
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn与稀H2SO4反应:2Zn+2H+═2Zn2++H2↑ | |
| B. | 氯气和水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+═H2SiO3↓+2Na+ | |
| D. | 硫酸氢钠溶液与过量氢氧化钡溶液混合:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 己知反应:2Al(l) $\stackrel{催化剂}{?}$B(l)△H=-QkJ/mol,取等量A分别在0℃和20℃下反应,测得其转化率Y随时间t变化的关系曲线(Y-t)如图所示.下列说法正确的是( )
己知反应:2Al(l) $\stackrel{催化剂}{?}$B(l)△H=-QkJ/mol,取等量A分别在0℃和20℃下反应,测得其转化率Y随时间t变化的关系曲线(Y-t)如图所示.下列说法正确的是( )| A. | a代表20℃下A的Y-t曲线 | |
| B. | 反应到66min时,0℃和20℃下反应放出的热量相等 | |
| C. | 0℃和20℃下达到平衡时,反应都放出QkJ热量 | |
| D. | 反应都达到平衡后,正反应速率a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室某浓硫酸的试剂瓶上的标签如右图所示,根据标签上的有关数据回答下列问题:
实验室某浓硫酸的试剂瓶上的标签如右图所示,根据标签上的有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
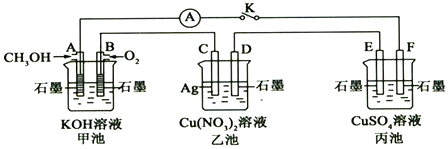
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com