
| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
| 0 min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | |||
| 20min | 1 | |||
| 30min | 1 |
分析 Ⅰ、已知:H2的热值为142.9KJ•g-1,燃烧热为285.8KJ/mol,
①H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8KJ/mol
②N2(g)+2O2(g)=2NO2(g)△H=+133kJ•mol-1
③H2O(g)=H2O(l)△H=-44kJ•mol-1
依据盖斯定律计算可以计算要求反应的焓变,再根据热化学方程式的书写方法得到热化学方程式即可;
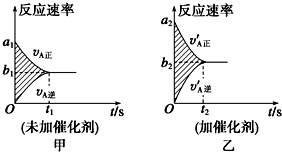
Ⅱ、(1)催化剂只改变正逆化学反应的速率,缩小达到平衡的时间,但转化率不变,以此来解答即可;
(2)反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,可由此进行判断;
(3)①达到平衡状态时,各组分的浓度不随时间的变化而变化,据此回答;②根据三行式计算结合反应速率等于浓度变化量和时间变化量的比值、转化率等于变化量和初始量的比值来计算;③影响反应速率的因素:浓度减小,反应速率减慢,反之加快;影响化学平衡移动的因素:增大反应物的浓度,平衡正向移动,减小反应物浓度,反应逆向移动.
解答 解:Ⅰ. 已知:H2的热值为142.9KJ•g-1,燃烧热为285.8KJ/mol,
①H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8KJ/mol
②N2(g)+2O2(g)=2NO2(g)△H=+133kJ•mol-1
③H2O(g)=H2O(l)△H=-44kJ•mol-1
①×4-②-③×4得到催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1;
故答案为:4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1;
Ⅱ、(1)催化剂只改变反应速率,缩小达到平衡的时间,但转化率不变,
乙图使用催化剂,反应速率加快,故a1<a2,即①错误,②正确;
乙图使用催化剂,反应速率加快,故b1<b2,即③错误,④正确;
时间缩短,所以t1>t2,即⑤正确,⑥错误;
阴影面积为反应物浓度的变化,由于催化剂不影响平衡移动,则两图中阴影部分面积相等,故⑦正确,⑧错误;
即正确的为②④⑤⑦,
故选B;
(2)a、混合气体的平均相对分子质量等于质量和物质的量的比值,反应前后质量守恒,物质的量变化,故混合气体的平均相对分子质量变化,当混合气体的平均相对分子质量保持不变,达到了平衡,故a正确;
b、CO2和H2的体积分数保持不变,说明正逆反应速率相等,达到了平衡状态,故b正确;
c、CO2和H2的转化率相等,不能说明正逆反应速率相等,不一定达到了平衡状态,故c错误;
d、混合气体的密度等于气体质量和体积的比值,反应前后质量守恒,体积不变,所以密度始终不变,当密度保持不变的状态不一定是平衡状态,故d错误;
e、1mol CO2生成的同时有3mol H-H键断裂,能说明正逆反应速率相等,一定达到了平衡状态,故e正确,
故选abe;
(3)①根据图示知道,从20min到30min时各物质的浓度没有发生改变,所以30min时,反应到达平衡状态,
故答案为:是;从20min到30min时各物质的浓度没有发生改变;
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)起始量(mol)
2 6 0 0
变化量(mol) 1 3 1 1
30min量(mol) 1 3 1 1
对反应I,前10min内的平均反应速率v(CH3OH)=$\frac{1}{3}$ v(H2)=$\frac{1}{3}$×(6-4.5)mol2L10min=0.025mol•L-1•min-1;平衡时H2的浓度c(H2)=1.5mol•L-1,平衡时CO2的转化率=50%,故答案为:0.025mol•L-1•min-1;1.5mol•L-1;50%;
③在其它条件不变下,若20min时往密闭容器中通入1mol氖气,此时各组分的浓度不变,所以该反应速率不变,若20min时往密闭容器中通入1mol氢气,此时氢气的浓度增大,该反应速率将变大,故答案为:不变;变大.
点评 本题考查了热化学方程式书写,平衡影响因素分析判断,平衡计算的分析应用,注意恒温恒容和恒容绝热容器的分析判断,掌握基础是关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 稀释 pH=4的醋酸,溶液中c(OH-)离子的浓度降低 | |
| B. | pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7 | |
| C. | 0.2 mol/L的盐酸与等体积水混合后pH=1 | |
| D. | 分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一定条件下2L的密闭容器中,反应aA(g)+bB(g)?cC(g)+dD(g)达到平衡.
一定条件下2L的密闭容器中,反应aA(g)+bB(g)?cC(g)+dD(g)达到平衡.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | z=4 | B. | B的转化率是40% | ||
| C. | A的平衡浓度是1.4 mol•L-1 | D. | 平衡时气体压强是原来的1.2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 698K时,向某V L的密闭容器中充入2mol H2(g)和2mol I2(g),发生反应:H2(g)+I2(g)=2HI(g)△H=-26.5kJ•mol-1,测得各物质的物质的量浓度与时间变化的关系如图所示.
698K时,向某V L的密闭容器中充入2mol H2(g)和2mol I2(g),发生反应:H2(g)+I2(g)=2HI(g)△H=-26.5kJ•mol-1,测得各物质的物质的量浓度与时间变化的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由C(s,石墨)═C(s,金刚石)△H=+119 kJ•mol-1可知,金刚石比石墨稳定 | |
| C. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 molNaOH的稀溶液混合,放出的热量大于57.3 kJ | |
| D. | 在25℃、101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量.则这些氢气完成燃烧生成气态水时,放出的热量比285.8 kJ还要多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 短周期元素中,最外层电子数是其电子层数两倍的元素共有3种 | |
| B. | 第三周期元素的离子半径大小比较:S2->Cl->Na+>Mg2+>Al3+ | |
| C. | 日本核电站释放出的131I、132I和133I属于同素异形体 | |
| D. | 相同条件下,测定同浓度的Na2CO3溶液和Na2SO4溶液的pH,可比较C和S的非金属性强弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com