
正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如下图)。
 下列有关说法正确的是( )
下列有关说法正确的是( )
A.正硼酸晶体中只存在氢键
B.H3BO3分子的稳定性与氢键无关
C.分子中硼原子最外层为8e— 稳定结构
D.含1molH3BO3的晶体中有6mol氢键
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
已知:2H2(g)+O2(g)====2H2O(l) ΔH=-571.6 kJ·mol-1
CH4(g)+2O2(g)====CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1
现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3 695 kJ,则原混合气体中H2与CH4的物质的量之比是( )
A. 1∶1 B.1∶3 C.1∶4 D.2∶3
1∶1 B.1∶3 C.1∶4 D.2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.元素周期表中的ⅠA族和ⅦA族元素间所形成的化学键可能是共价键也可能是离子键
B.H—O键键能为463KJ∕mol,即1molH2O分解成H2和O2时,消耗能量为2×463KJ
C.分子中键能越大,键长越长,则分子越稳定
D.水分子可表示为H—O—H,分子中键角为180°
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z三种元素,原子序数依次减小。X是第四周期主族元素,其部分电离能如图1所示;X、Y元素具有相同的最高正化合价;Z原子价电子排布式nsnnpn。回答下列问题:
(1)X原子的电子排布式为___________。
(2)电负性:X ______Y(填“>”、“=”或“<”)。
(3)元素Z的一种氢化物(化学式为Z2H4)是重要的
化工原料。有关Z2H4分子的说法正确的是______(填字母)。
A.Z的原子与氢原子形成的化学键可以旋转 B.不含非极性键
C.分子中含有氢键 D.含有4个σ键和1个π键
(4)NH4Cl晶体中含有多种化学键,其中一定不含有的化学键是_____ (填字母)。
A.离子键 B.极性键 C.配位键 D.金属键
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列溶液中,能大量共存的离子组是( )
A.能使pH试纸显蓝色的溶液中:
B.常温下 的溶液中:
的溶液中:
C.含有大量Al3+的溶液中:
D.常温下pH为7的溶液中: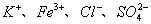
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用标准盐酸测定未知浓度NaOH溶液,用甲基橙作指示剂,下列操作可能使测定结果偏低的是( )
A.酸式滴定管在装酸液前未用标准酸液润洗
B.开始时酸式滴定管尖嘴部分留有气泡,滴定过程中消失
C.锥形瓶内溶液颜色由黄变橙时立即停止滴定
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
查看答案和解析>>
科目:高中化学 来源: 题型:
用可溶性钡盐检验SO42-离子的存在时,先在待测溶液中加入盐酸,其作用是 ( )
A.形成较多的白色沉淀 B.排除SO42-以外的其它阴离子及Ag+的干扰
C.形成的沉淀纯度更高 D.排除Ba2+以外的其它阳离子的干扰
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是锌、铜和稀硫酸形成的原电池,下列叙述不合理的是
A.溶液中H+向Zn电极移动
B.外电路中电流方向为:Cu→Zn
C.负极上的电极反应:Zn-2e-===Zn2+
D.有1 mol电子流过导线,则Cu电极上产生的H2为11.2 L(标准状况)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com