
铁是人类应用较早,当前应用量最大的金属元素。下列有关铁及其化合物的有关说法中正确的是( )
A.赤铁矿的主要成分是Fe3O4
B.铁与水蒸气在高温下的反应产物为Fe2O3和H2
C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤
D.Fe3+与KSCN产生血红色沉淀
科目:高中化学 来源: 题型:
下面是新设的一组垃圾箱的说明:
| 厦门市生活垃圾分类 | ||
| 可回收垃圾 | 不可回收垃圾 | 有害垃圾 |
| 1.纸类 2.玻璃 3.金属 4.塑料 5.橡胶 6.纺织品 | 1.厨房垃圾 2.灰土 3.杂草 4.枯枝 5.花卉 | 1.日光灯管 2.电池 3.喷雾罐 4.指甲油瓶 5.药品药瓶 6.涂改液瓶 |
(1)小明在整理房间时,清理出如下物品,它们应分别放入哪个垃圾箱(请填序号):
A.废作业本;B.汽水易拉罐;C.生锈铁钉;D.矿泉水瓶;
E.烂苹果;F.涂改液瓶
应放入“可回收垃圾箱”的是:___________________________________ _____________________________________;
应放入“不可回收垃圾箱”的是:__________________________________ ______________________________________;
应放入“有害垃圾箱”的是:______________________________________ __________________________________。
(2)小明用盐酸除去铁钉上的锈(主要成分为氧化铁)以重新使用它,请写出盐酸除锈的化学方程式:_____________________________________________ _____________________________________________________________。
(3)废铜有两种回收方法:
方法一:Cu+4HNO3===Cu(NO3)2+2X↑+2H2O(X是一种大气污染物)
方法二:铜在空气中加热生成氧化铜,氧化铜再与盐酸反应生成氯化铜和水。
①方法一中,X的化学式为:__________;
方法二的优点是:_________________________________________;
②请写出从氯化铜溶液中提取铜的化学方程式:_____________________________________________________________________________________________________________________;
该反应属于化学反应的基本类型是___________________________________ _____________________________________。
(4)请从可回收垃圾的类别中,举例说说化学的研究成果给社会进步带来的贡献:_______________________________________________________ _________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y、Z三种有机物,按要求回答下列问题:
(1)取3.0 g有机物X,完全燃烧后生成3.6 g水和3.36 L CO2(标准状况),已知该有机物的蒸气对氢气的相对密度为30,求该有机物的分子式:____________________________。
(2)有机物Y的分子式为C4H8O2,其红外光谱图如下:

则该有机物的可能结构为__________(填字母)。
A.CH3COOCH2CH3 B.CH3CH2COOCH3
C.HCOOCH2CH2CH3 D.(CH3)2CHCOOH
(3)有机物Z的结构可能有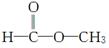 和
和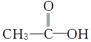 两种,为对其结构进行物理方法鉴定,可用__________或__________。
两种,为对其结构进行物理方法鉴定,可用__________或__________。
①有机物Z若为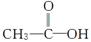 ,则红外光谱中应该有__________个吸收峰;核磁共振氢谱中应有__________个峰。
,则红外光谱中应该有__________个吸收峰;核磁共振氢谱中应有__________个峰。
②有机物Z若为 ,则红外光谱中应该有__________个吸收峰;核磁共振氢谱中应有________个峰。
,则红外光谱中应该有__________个吸收峰;核磁共振氢谱中应有________个峰。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子在指定溶液中能大量共存的是( )
A.1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO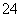
B.1.0 mol·L-1的FeCl2溶液:NO 、Na+、K+、ClO-
、Na+、K+、ClO-
C.使酚酞变红的溶液中:Na+、Cl-、SO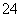 、Fe3+
、Fe3+
D.酸性溶液中:NO 、SO
、SO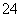 、Fe3+、Mg2+
、Fe3+、Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及其化合物是中学化学中的一类重要物质,下列关于铁元素的叙述中正确的是( )
A.2Fe3++Fe===3Fe2+成立说明氧化性:Fe3+>Fe2+
B.25 ℃,pH=0的溶液中,Al3+、NH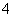 、NO
、NO 、Fe2+可以大量共存
、Fe2+可以大量共存
C.5.6 g铁与足量的氯气反应失去电子为0.2 mol
D.硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+===Fe3++4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某校探究性学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如下:
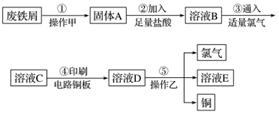
请回答下列问题:
(1)步骤①中先加入热的Na2CO3溶液除油污,操作甲的名称是________。
(2)步骤②中,除发生反应Fe+2HCl===FeCl2+H2↑外,其他可能反应的离子方程式为________________。
(3)溶液C的颜色是________,溶液D中可能含有的金属阳离子有________。
(4)可以验证溶液B中是否含有Fe2+的一种试剂是______(填字母)。
a.稀硫酸 b.铁 c.硫氰化钾 d.酸性高锰酸钾溶液
(5)操作乙的名称是________,步骤⑤产生金属铜的化学方程式为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
近日国内知名山茶油品牌“金浩茶油”被多家媒体曝光致癌物苯并(a)芘含量超标。苯并(a)芘是一种致癌物、致畸原及诱变
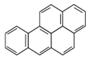
剂,也是多环芳烃中毒性最大的一种强致癌物。苯并(a)芘的结构简式如图所示,下列有关苯并(a)芘的说法中不正确的是( )
A.苯并(a)芘的分子式为C20H12,属于稠环芳香烃
B.苯并(a)芘与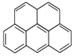 互为同分异构体
互为同分异构体
C.苯并(a)芘在一定条件下可以发生取代反应,能使酸性KMnO4溶液褪色
D.苯并(a)芘不易溶于水,易溶于苯、氯仿等有机溶剂
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化氯(ClO2)是一种高效、广谱、安全的杀菌消毒剂。
(1)氯化钠电解法是一种可靠的工业生产ClO2的方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO 等杂质。除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO
等杂质。除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO ,其原因是________________________________________________________________________。
,其原因是________________________________________________________________________。
[已知:Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=5.1×10-9]
②该法工艺原理如下图。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。

工艺中可以利用的单质有________(填化学式),发生器中生成ClO2的化学方程式为________________________________________________________________________。
(2)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2。完成反应的化学方程式:
 __(D)__+24NaClO3+12H2SO4===
__(D)__+24NaClO3+12H2SO4=== ClO2↑+
ClO2↑+ CO2↑+18H2O+
CO2↑+18H2O+ ________
________
(3)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含CN-相同量的电镀废水,所需Cl2的物质的量是ClO2的________倍。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com