
下列化合物中含有2个手性碳原子的是( )
|
| A. |
| B. |
| C. | CF2Cl2 | D. |
|
考点:
常见有机化合物的结构.
专题:
有机化学基础.
分析:
手性碳原子指连有四个不同基团的碳原子,手性碳原子判断注意:1、手性碳原子一定是饱和碳原子;2、手性碳原子所连接的四个基团要是不同的.
解答:
解:A、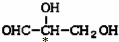 只有如图标记“*”的碳原子连接四个不同的基团,是手性碳原子,含有1个手性碳原子,故A不符合;
只有如图标记“*”的碳原子连接四个不同的基团,是手性碳原子,含有1个手性碳原子,故A不符合;
B、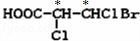 如图标记“*”的碳原子连接四个不同的基团,是手性碳原子,含有2个手性碳原子,故B符合;
如图标记“*”的碳原子连接四个不同的基团,是手性碳原子,含有2个手性碳原子,故B符合;
C、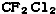 中C原子连接两种原子,不存在手性碳原子,故C不符合;
中C原子连接两种原子,不存在手性碳原子,故C不符合;
D、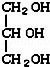 中间碳原子连接1个﹣OH、1个﹣H、2个CH2OH,不是手性碳原子,两端的碳原子连接了2个﹣H,不手性碳原子,分子中不存在手性碳原子,故D不符合.
中间碳原子连接1个﹣OH、1个﹣H、2个CH2OH,不是手性碳原子,两端的碳原子连接了2个﹣H,不手性碳原子,分子中不存在手性碳原子,故D不符合.
故选:B.
点评:
考查手性碳原子的判断,比较基础,手性碳原子判断注意:1、手性碳原子一定是饱和碳原子;2、手性碳原子所连接的四个基团要是不同的.


科目:高中化学 来源: 题型:
用20g烧碱配制成500mL其物质的量浓度为1mol/L,从中取出1mL,其物质的量浓度为 mol/L;含溶 质 g.若将这1mL溶液用水稀释到100mL,所得溶液中溶质的物质的量浓度为 mol/L,其中含Na+ .
查看答案和解析>>
科目:高中化学 来源: 题型:
A﹣H分别是中学化学中的常见物质,它们之间有下图所示关系(反应中所需要和所生成的水均没有列出),已知B、H为常见的金属单质,A、C均为气体单质且A气体的颜色为黄绿色,F的水溶液为蓝色,B、D、G、E中均含同一种元素.请回答:
(1)A、B、G、H分别是什么物质?(写物质名称)
A ,B铁,G ,H
(2)写出D→F反应的离子方程式: .
(3)写出G和稀盐酸反应的化学方程式: .
(4)2molB与足量的A完全反应生成D时所转移的电子为 mol.
(5)如何检验D溶液中的阳离子? .

查看答案和解析>>
科目:高中化学 来源: 题型:
人们常将在同一原子轨道上运动的,自旋方向相反的2个电子,称为“电子对”;将在同一原子轨道上运动的单个电子,称为“未成对电子”.以下有关主族元素原子的“未成对电子”的说法,错误的是( )
|
| A. | 核外电子数为奇数的基态原子,其原子轨道中一定含有“未成对电子” |
|
| B. | 核外电子数为偶数的基态原子,其原子轨道中一定不含“未成对电子” |
|
| C. | 核外电子数为偶数的基态原子,其原子轨道中可能含有“未成对电子” |
|
| D. | 核外电子数为奇数的基态原子,其原子轨道中可能不含“未成对电子” |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知SO3、BF3、CCl4、PCl5、SF6都是非极性分子,而H2S、NH3、NO2、SF4、BrF5都是极性分子,由此可推出ABn型分子属于非极性分子的经验规律是( )
|
| A. | ABn型分子中A、B均不含氢原子 |
|
| B. | A元素的相对原子质量必小于B元素的相对原子质量 |
|
| C. | 分子中所有原子都在同一平面上 |
|
| D. | ABn型的价层电子对数等于n |
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素.
| a |
| ||||||||||||||||
| b | c | d | e | f |
| ||||||||||||
| g | h | i | j | k | l | m |
| ||||||||||
| n | o |
试回答下列问题:
(1)请写出字母O代表的元素符号 ,该元素在周期表中的位置 .
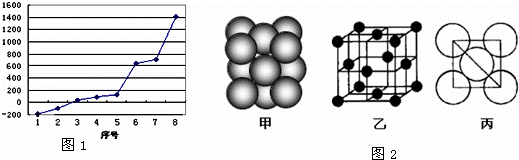
(2)第三周期8种元素按单质熔点高低的顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填如图1中的序号).
(3)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是 (填化学式),试从结构角度加以解释: .
(4)k与l形成的化合物kl2的电子式是 ,它在常温下呈液态,形成晶体时,属于 晶体.
(5)i单质晶体中原子的堆积方式如图2(甲)所示,其晶胞特征如图2(乙)所示,原子之间相互位置关系的平面图如图2(丙)所示.若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
一个晶胞中i原子的数目为 ,该晶体的密度_ (用M、NA、d表示).
(6)a与d构成的阳离子和i的阳离子可与硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入浓氢氧化钡溶液,产生的现象有:①溶液中出现白色沉淀并伴有有刺激性气味气体放出,②沉淀逐渐增多后又逐渐减少直至最终沉淀的量不变.写出沉淀的量不变时发生反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是()
A. 澄清的石灰水与稀盐酸反应Ca(OH)2+2H+═Ca2++2H2O
B. 钠与水的反应Na+2H2O═Na++2OH﹣+H2↑
C. 硫酸氢钠溶液与少量氢氧化钡溶液混合:2H++SO42﹣+Ba2++2OH﹣═BaSO4↓+2H2O
D. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
在Na+浓度为0.5mol•L﹣1的某澄清溶液中,还可能含有下表中的若干种离子.
阳离子 K+Ag+Mg2+Ba2+
阴离子 NO3﹣、CO32﹣、SiO32﹣、SO42﹣
现取该溶液100mL进行如下实验(气体体积均在标准状况下测定).
序号 实验内容 实验结果
Ⅰ 向该溶液中加入足量稀盐酸 产生白色沉淀并放出标准状况下0.56L气体
Ⅱ 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 固体质量为2.4g
Ⅲ 向Ⅱ的滤液中滴加BaCl2溶液 无明显现象
请回答下列问题.
(1)实验Ⅱ,混合液过滤后如何洗涤沉淀? .
(2)澄清溶液中一定不存在的离子是 .
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,填写表中阴离子的物质的量浓度(能计算出结果的填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)
阴离子 NO3﹣ CO32﹣ SiO32﹣ SO42﹣
c/mol•L﹣1 ?
(4)判断K+是否存在,若存在,求其最小浓度,若不存在,请说明理由: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com