

| A. | 该硫酸的浓度为9.2 mol•L-1 | |
| B. | 配制480 mL 4.6 mol•L-1的稀硫酸需该H2SO4 125mL | |
| C. | 该硫酸与等体积水混合质量分数变为49% | |
| D. | 取该硫酸100 mL,则浓度变为原来的$\frac{1}{5}$ |
分析 A.c(H2SO4 )=$\frac{1000ρω}{M}$;
B.配制480mL稀硫酸需要配制500mL容量瓶,需要配制500mL,溶液稀释前后溶质的物质的量不变;
C.硫酸的密度大于水,等体积硫酸、水混合后溶液的质量小于原硫酸的质量2倍;
D.溶液是均匀的,取出溶液的浓度与原溶液浓度相等.
解答 解:A.c(H2SO4 )=$\frac{1000ρω}{M}$=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,故A错误;
B.配制480mL稀硫酸需要配制500mL容量瓶,需要配制500mL,溶液稀释前后溶质的物质的量不变,配制500mL溶液需要硫酸的物质的量=4.6mol/L×0.5L=2.3mol,需要浓硫酸体积=$\frac{2.3mol}{18.4mol/L}$=125mL,故B正确;
C.硫酸的密度大于水,等体积硫酸、水混合后溶液的质量小于原硫酸的质量2倍,故混合后的质量分数大于49%,故C错误;
D.溶液是均匀的,取出溶液的浓度与原溶液浓度相等为18.4mol/L,溶液中溶质的物质的量变为原溶液中的$\frac{1}{5}$,故D错误;
故选B.
点评 本题考查物质的量浓度有关计算,涉及物质的量浓度、质量分数等,难度不大,注意理解掌握物质的量浓度与质量分数之间的关系,易错选项是B.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铜作负极 | B. | 锌作正极 | ||
| C. | 电子由铜经导线流向锌 | D. | 锌片上的反应为:Zn-2e-=Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 灯光明暗程度不变 | B. | 灯光变暗 | ||
| C. | 灯光明暗程度变化不明显 | D. | 灯光变亮 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 品名 | 蔬菜苏打饼 |
| 配料 | 面粉、鲜鸡蛋、精炼食用植物油、白砂糖、奶油、食盐、脱水青菜、橙汁 |
| 保质期 | 十二个月 |
| 生产日期 | 2016 年8月20日 |
| A. | 富含蛋白质的是鸡蛋 | |
| B. | 富含维生素的是脱水青菜和橙汁 | |
| C. | 富含糖类的物质只有白砂糖 | |
| D. | 富含油脂的是精炼食用植物油和奶油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+ | B. | Ba2+ | C. | Cl- | D. | Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
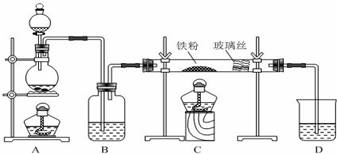
 某探究小组采用如图所示装置进行Fe粉与水蒸气的反应.
某探究小组采用如图所示装置进行Fe粉与水蒸气的反应.| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,无气泡 |
| 2 | 取步骤1中溶液,滴加酸性KMnO4溶液 | 紫色褪去 | 紫色褪去 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com