
| A. | 无沉淀生成,溶液显红色 | B. | 无沉淀生成,溶液显无色 | ||
| C. | 有沉淀生成,溶液显无色 | D. | 有沉淀生成,溶液显红色 |
科目:高中化学 来源: 题型:多选题
| A. | 1molP4含有p-p键的个数为4NA | |
| B. | 1molSiC中含有C-Si键的个数为2NA | |
| C. | 含C为1mol的金刚石中含有C-C键的个数为2NA | |
| D. | 1molSi02中含Si-O键的个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ba2+、SO42-、Cl- | B. | H+、Ag+、Cl-、NO3- | ||
| C. | K+、H+、CO32-、Cl- | D. | Na+、Mg2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,此烃名称为3-甲基-2-乙基-1-戊烯.
,此烃名称为3-甲基-2-乙基-1-戊烯.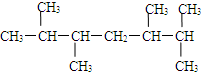 ,其一氯代物有5种.
,其一氯代物有5种.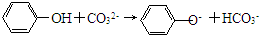 ,之后再进行分液操作.
,之后再进行分液操作.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数:C>d | B. | 离子还原性:Y>Z | C. | 稳定性:H2Y>HZ | D. | 原子半径:X<W |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com