
| A、HB的电离方程式为:HB═H++B- |
| B、NaB溶液中:c(Na+)>c(B-)>c(H+)>c(OH-) |
| C、NaB溶液中存在如下关系:c(Na+)+c(H+)═c(HB)+c(B-) |
| D、0.1mol/L NaB溶液中水电离的OH-浓度大于10-7mol/L |


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:
| A、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ | ||||
| B、Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH-+O2↑ | ||||
| C、将氯气溶于水制备次氯酸:Cl2+H2O=2H++Cl-+ClO- | ||||
D、用惰性电极电解饱和氯化钠溶液:2Cl-+2H+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
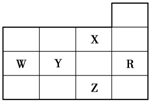
| A、其气态氢化物的稳定性是X>Y>W>Z |
| B、其最高价氧化物对应的水化物的酸性:Y>W |
| C、电负性、第一电离能的大小顺序都是X>Y>W |
| D、Y、Z的阴离子电子层结构都与R原子的相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2 |
| B、Cl2O |
| C、ClO2 |
| D、Cl2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是物质的质量单位 |
| B、物质的量是国际单位制中七个基本单位之一 |
| C、阿伏加德罗常数是12 g 12C中含有的碳原子数目 |
| D、标准状况下,1 mol H2O所占的体积为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解质:明矾、冰醋酸、硫酸钡 |
| B、酸性氧化物:CO2、SO2、NO、SiO2 |
| C、混合物:铝热剂、矿泉水、水玻璃、漂白粉 |
| D、同素异形体:C60、C70、金刚石 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸溶于水:CH3COOH=CH3COO-+H+ |
| B、熔融状态下的NaHSO4:NaHSO4=Na++H++SO42- |
| C、碳酸氢钠溶于水:HCO3-+H2O?CO32-+H3O+ |
| D、硫化氢溶于水:H2S?2H++S2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com