
��8�֣�������أ�K2FeO4����һ�����͡���Ч�������ɫˮ����������C12��O3��ClO2��KMnO4�����Ը�ǿ��������Ⱦ����ҵ�������Ƶø������ƣ�Ȼ���ڵ����£������������Һ�м���KOH�����ͣ�ʹ�������������
��1��ʪ���Ʊ��������ƣ�Na2FeO4���ķ�Ӧ��ϵ��������:Fe��OH��3��ClO�D��OH�D��FeO42�D��Cl�D��H2O��
��д������ƽʪ���Ʊ��������Ƶ����ӷ���ʽ�� _____ ��
�ڵ����£��ڸ���������Һ�м���KOH�����Ϳ�����������أ�K2FeO4��������ܵ�ԭ���� ��
��2���ɷ��Ʊ��������Ƶ���Ҫ��ӦΪ��2FeSO4+6Na2O2��2Na2FeO4+2Na2O+2Na2SO4+O2����
�÷�Ӧ�еĻ�ԭ���� ������l mol Na 2FeO4ת�� mol���ӡ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ���ء����ء����ء�᪱���У�����ڶ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
Ϊ�ᴿ��������(�����ڵ�����������)����ѡ�õij����Լ��ͷ�������ȷ����
ѡ�� | ���ᴿ������ | �����Լ� | ���ӷ��� |
A | �廯����Һ(NaI) | ��ˮ��CCl4 | ��ȡ����Һ |
B | �Ȼ����Һ(FeCl3) | ����������Һ | ���� |
C | ������̼(CO) | ����ͭ��ĩ | ͨ�����ȵ�CuO��ĩ |
D | ��������(����) | �Ҵ���Ũ���� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ��10�½β⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
���и���ʵ��������������ó��Ľ��۴������
ѡ�� | ʵ����� | ʵ������ | ���� |
A | ����ҺX���ȵμ�ϡ���ᣬ�ٵμ�Ba(NO3)2��Һ | ���ְ�ɫ���� | ��ҺX��һ������SO42�� |
B | ��FeCl3+3KSCN | ��ϵ��ɫ�ޱ仯 | KCl����ʹ��ƽ���ƶ� |
C | �����KI��Һ�в���ͨ��C12 | ��Һ�ȱ�������ɫ | C12�Ƚ�I-����ΪI2��������ֽ�I2������ |
D | �����ݵ�������Һ�зֱ�μӱ���NaCl��Һ��CuSO4��Һ | ���й������� | �����ʾ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������벻�����ֻ�ѧ���ʣ�����˵������ȷ����
�ٶ��������ǵ��ӹ�ҵ�г��õİ뵼�����
������������������������
���������ռ���Һ��ʯ���鷴Ӧ���ܵõ�����������
����Ȼ����ʯ�ͺ�ú�����ڲ���������Դ
����ʳ����ϴ��ˮƿ�е�ˮ��
���ô�����Һϴ�Ӳ;��ϵ�����
�����������麬�����еĵ����
��ҽ���Ͽ���̼�ᱵ��x�����ӳ�θ���ڷ�ҩ������Ϊ̼�ᱵ������ˮ
��ij��ˮ��Ʒ����һ��ʱ���pH��4.68��Ϊ4.00������Ϊˮ���ܽ��CO2����
��ӵ�ʳ�������ӵ���ض����õ⻯�أ�����Ϊ�����������ˮ���⻯�ز�����ˮ
A���٢ۢܢߢ� B���ڢۢܢݢ� C���٢ߢ��� D���٢ڢܢߢ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ�ڵ�����ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ��CO2�����ԭΪCH4�Ĺ���ԭ��ʾ��ͼ������˵������ȷ����
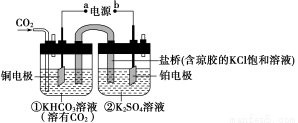
A���ù����ǵ���ת��Ϊ��ѧ�ܵĹ���
B��һ��ʱ��ٳ���n(KHCO3)����
C��һ��ʱ��ڳ�����Һ��pHһ���½�
D��ͭ�缫�ĵ缫��ӦʽΪCO2��8H����8e��===CH4��2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
��14�֣��������ƣ�NaClO2������ҪƯ����̽��С�鿪չ����ʵ�飬�ش��������⣺
ʵ�����ȡNaClO2���尴����ͼװ�ý�����ȡ��
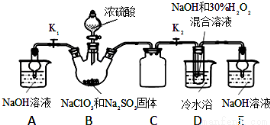
��֪��NaClO2������Һ�ڵ���38��ʱ����NaClO2•3H2O������38��ʱ����NaClO2������60��ʱNaClO2�ֽ��NaClO3��NaCl��
��1��װ��C�������� ��
��2����֪װ��B�еIJ�����ClO2���壬��װ��B�з�Ӧ�ķ���ʽΪ ��װ��D�з�Ӧ����NaClO2�Ļ�ѧ����ʽΪ ����Ӧ�����Һ�������ӳ���ClO2����ClO3����Cl����ClO����OH������ܺ��е�һ���������� ����������ӵķ����� ��
��3���벹���װ��D��Ӧ�����Һ�л��NaClO2����IJ������裮
�ټ�ѹ��55�������ᾧ���� ���� ���� �õ���Ʒ��
��4�������ȥD�е���ˮԡ�����ܵ��²�Ʒ�л��е������� ��
ʵ�����Ʒ���ʷ����봿�Ȳⶨ
��5���ⶨ��Ʒ��NaClO2�Ĵ��ȣ��ⶨʱ��������ʵ�飺
ȷ��һ����������Ʒ��������������ˮ������KI���壬�����������·������·�Ӧ��ClO2��+4I��+4H+=2H2O+2I2+Cl���������û��Һϡ�ͳ�100mL������Һ��ȡ25.00mL������Һ�����������Һ��ָʾ������c mol•L��1 Na2S2O3��Һ�ζ����յ㣬������ı���Һ�����ƽ��ֵΪV mL����֪��I2+2S2O32��=2I��+S4O62���������������ȡ����Ʒ��NaClO2�����ʵ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ���ϰ�У������ѧ�ڵ�һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
NAΪ�����ӵ�������ֵ������˵����ȷ����
A��1 L 0��1 mol/LNaHSO4��Һ�к���HSO4-����Ϊ0.1NA
B��16g16O2��18 g18O2�к��е���������Ϊ8NA
C��1 mol Fe��������ϡ���ᷴӦ��ת�Ƶ�����Ϊ2NA
D����״���£�2. 24 L Cl2����ˮ������Һ�к��е���������Ϊ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶������в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
 I���������Ƽ����й�
I���������Ƽ����й� I��˵����ȷ����
I��˵����ȷ����
A��������Ϊ131 B��������Ϊ131
C��������53 D��������53
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�£�H2N��NH2����һ�ָ���ȼ�ϣ��йػ�ѧ��Ӧ�������仯��ͼ��ʾ����֪����1mol��ѧ�������������kJ����N��NΪ942��O=OΪ500��N��NΪ154�������1molN��H�������������kJ����
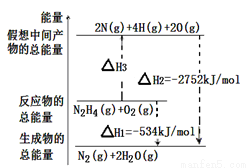
A��194 B��391 C��516 D��658
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com