
【题目】用4×10-3 mol的KZO4 恰好将60 mL 0.1 mol/L的Na2SO3溶液氧化为Na2SO4,则元素Z在还原产物中的化合价是
A. +6 B. +4 C. +3 D. +2
科目:高中化学 来源: 题型:
【题目】实验是化学的灵魂,是学好化学的重要情节。
Ⅰ.选取下列实验方法分离物质,将最佳分离方法的字母填在横线上。
A.萃取 B.升华 C.分液 D.蒸馏 E.过滤
(1)分离水和汽油的混合物:_______________。
(2)分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物:___。
Ⅱ.实验室欲配置480ml0.1mol·L-1NaOH溶液。
(3)通过计算得知:用托盘天平称取得NaOH质量为__________。在下图所示仪器中,配制上述溶液需要的仪器有_______________(填字母),除图中已有的仪器外,配置上述溶液还需要的玻璃仪器有胶头滴管和____________。
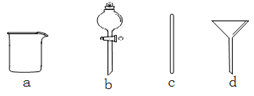
(4)配置时,其正确的操作顺序是________________(用字母表示,每个操作只用一次)。
A.用少量蒸馏水洗涤烧杯2-3次,洗涤液均注入容量瓶中,振荡
B.将称好的NaOH固体加入烧杯中,用适量蒸馏水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.盖好瓶盖,反复上下颠倒,摇匀
E.继续往容量瓶中加入蒸馏水,直到液面接近容量瓶颈刻度1-2cm处
F.改用胶头滴管滴加蒸馏水,使溶液凹液面恰好与刻度相切
(5)下列操作会造成所配NaOH溶液浓度偏低的是___________(填字母)
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某2 L恒容密团容器中充入2 mol X(g)和1mol Y(g)发生反应:2X(g)+ Y(g)![]() 3Z(g)△H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示:下列推断正确的是
3Z(g)△H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示:下列推断正确的是

A. Q点时,Y的转化率最大
B. 升高温度,平衡常数增大
C. W点Y的正反应速率等于M点Y的正反应速率
D. 平衡时充入Z.达到新平衡时Z的体积分数比原平衡时大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500 mL NH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A. (![]() -
-![]() ) mol/L B. (2b-a) mol/L
) mol/L B. (2b-a) mol/L
C. (5b-![]() ) mol/L D. (10b-5a) mol/L
) mol/L D. (10b-5a) mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000 molL-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且半分钟不变色,测得所耗盐酸的体积为V1mL。
④重复以上过程两次,但在重复第一次时滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。
试回答下列问题:
(1)锥形瓶中的溶液从 _________色变为______ 色时,停止滴定。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察 ____________
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是 ______________________,由此造成的测定结果 _________________(偏高、偏低或无影响)
(4)步骤②缺少的操作是 ________________________________
(5)下图,是某次滴定时的滴定管中的液面,其读数为 _____________mL
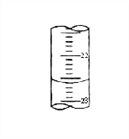
(6)V1 ______ V2 (填大于、小于、或等于)
(7)纠正错误以后实验测出下列数据:
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 4.00 | 24.10 |
第三次 | 25.00 | 0.50 | 23.40 |
请计算待测烧碱溶液的浓度:____________________ molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Fe、Cu、Fe2+、Fe3+和Cu2+盛于同一容器中充分反应,反应后Fe有剩余,则容器中其它存在的单质或离子只能是
A. Cu、Fe3+ B. Fe2+、Fe3+ C. Cu、Cu2+ D. Cu、Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a mol Na2O2和b mol NaHCO3固体混合后,在密闭容器中加热到250℃,使其充分反应,当排出气体为两种气体时,a︰b不可能为
A. 3︰4 B. 3︰2 C. 2︰3 D. 4︰5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表中对于相关物质的分类全部正确的是()
选项 | 纯净物 | 混合物 | 碱性氧化物 | 非电解质 |
A | 液氯 | 漂白粉 | Al2O3 | CO |
B | 醋酸 | 浓硫酸 | Na2O2 | 乙醇 |
C | 碱石灰 | 盐酸 | K2O | Cl2 |
D | 胆矾 | 水玻璃 | CaO | SO2 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+浓度为0.4 mol/L,SO42-的浓度为0.7 mol/L,则该溶液中K+的浓度为( )
A.0.1 mol/LB.0.15 mol/LC.0.2 mol/LD.0.25 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com