
| ±»Ģį“æµÄĪļÖŹ | ³żŌÓŹŌ¼Į | ·ÖĄė·½·Ø | |
| A | ŅŅĖįŅŅõ„£ØŅŅ“¼£© | ŅŅĖį | ¼ÓČČ»ŲĮ÷ |
| B | ŅŅĶé£ØŅŅĻ©£© | ĖįŠŌKMnO4 | Ļ“Ęų |
| C | ŅŅ“¼£ØŅŅĖį£© | ŠĀÖĘŃõ»ÆøĘ | ÕōĮó |
| D | ±½£Øä壩 | µā»Æ¼ŲČÜŅŗ | ·ÖŅŗ |
| A£® | A | B£® | B | C£® | C | D£® | D |
·ÖĪö A£®ŅŅĖįÓėŅŅ“¼µÄ·“Ó¦ĪŖæÉÄę·“Ó¦£»
B£®ŅŅĻ©±»øßĆĢĖį¼ŲŃõ»ÆÉś³É¶žŃõ»ÆĢ¼£»
C£®ŅŅĖįÓėCaO·“Ó¦ŗó£¬Ōö“óÓėŅŅ“¼µÄ·Šµć²īŅģ£»
D£®äåÓėKI·“Ӧɜ³ÉµÄµāŅ×ČÜÓŚ±½£®
½ā“š ½ā£ŗA£®ŅŅĖįÓėŅŅ“¼µÄ·“Ó¦ĪŖæÉÄę·“Ó¦£¬³żŌÓ²»³¹µ×£¬Ó¦Ń”±„ŗĶĢ¼ĖįÄĘČÜŅŗ”¢·ÖŅŗ·Ø·ÖĄė£¬¹ŹA“ķĪó£»
B£®ŅŅĻ©±»øßĆĢĖį¼ŲŃõ»ÆÉś³É¶žŃõ»ÆĢ¼£¬ŅżČėŠĀŌÓÖŹ£¬Ó¦Ń”äåĖ®”¢Ļ“Ęų£¬¹ŹB“ķĪó£»
C£®ŅŅĖįÓėCaO·“Ó¦ŗó£¬Ōö“óÓėŅŅ“¼µÄ·Šµć²īŅģ£¬Č»ŗóÕōĮóæÉ·ÖĄė£¬¹ŹCÕżČ·£»
D£®äåÓėKI·“Ӧɜ³ÉµÄµāŅ×ČÜÓŚ±½£¬ŅżČėŠĀŌÓÖŹ£¬Ó¦Ń”NaOHČÜŅŗ”¢·ÖŅŗ£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²é»ģŗĻĪļ·ÖĄėĢį“棬ĪŖøßĘµæ¼µć£¬°ŃĪÕÓŠ»śĪļµÄŠŌÖŹ”¢·¢ÉśµÄ·“Ó¦”¢»ģŗĻĪļ·ÖĄė·½·ØĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅā³żŌÓµÄŌŌņ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
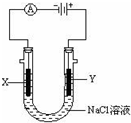
| A£® | øĆ×°ÖĆ·¢ÉśĮĖ»Æѧ±ä»Æ | B£® | øĆ×°ÖĆæÉ»ńµĆĀČĘų | ||
| C£® | øĆ×°ÖĆæÉ»ńµĆ½šŹōÄĘ | D£® | ČÜŅŗÖŠµÄNa+ĻņX¼«ŅĘ¶Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²»±ä | B£® | Ōö“ó | C£® | ¼õŠ” | D£® | ĪŽ·ØÅŠ¶Ļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻĖĪ¬ĖŲ”¢ÕįĢĒ”¢ĘĻĢŃĢĒŗĶÖ¬·¾ŌŚŅ»¶ØĢõ¼žĻĀ¶¼æÉ·¢ÉśĖ®½ā·“Ó¦ | |
| B£® | ÓĶÖ¬¶¼²»ÄÜŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ« | |
| C£® | ŹÆÓĶ·ÖĮó”¢ĆŗµÄøÉĮó¾łĪŖĪļĄķ±ä»Æ | |
| D£® | µķ·Ū”¢µ°°×ÖŹŗĶĢģČ»Ļš½ŗ¾łŹĒĢģČ»øß·Ö×Ó»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
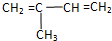 ¢Ż
¢Ż ¢ŽCH3CH£ØC2H5£©CH2CH£ØC2H5£©CH3¢ßC5H10¢ąClCHØTCHCl
¢ŽCH3CH£ØC2H5£©CH2CH£ØC2H5£©CH3¢ßC5H10¢ąClCHØTCHCl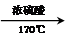 CH2ØTCH2”ü+H2O£®
CH2ØTCH2”ü+H2O£®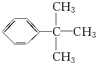 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ŹµŃéŠņŗÅ | ŹµŃé | ŹµŃéĻÖĻó | ½įĀŪ |
| ŹµŃé¢ņ | ½«ŹµŃé¢ńÖŠŹÕ¼Æµ½µÄĘųĢåµćČ¼ | ÄÜ°²¾²Č¼ÉÕ”¢²śÉśµĄ¶É«»šŃę | ĘųĢå³É·ÖĪŖ ¢ŁĒāĘų |
| ŹµŃé¢ó | Č”ŹµŃé¢ńÖŠµÄ°×É«²»ČÜĪļ£¬Ļ“µÓ£¬¼ÓČė×ćĮæ ¢ŚĻ”ŃĪĖį | ¢Ū²śÉśĘųÅŻ³ĮµķČ«²æČܽā | °×É«²»ČÜĪļæÉÄÜŗ¬ÓŠ²Ā²ā2ÖŠ²»ČÜĪļ |
| ŹµŃé¢ō | Č”ŹµŃé¢ńÖŠµÄ³ĪĒåŅŗ£¬ĻņĘäÖŠ¼ÓČėÉŁĮæCaCl2Ļ”ČÜŅŗ | ²śÉś°×É«³Įµķ | ČÜŅŗÖŠ“ęŌŚ ¢ÜCO32- |
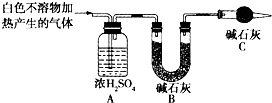
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł | B£® | ¢Ś | C£® | ¢Ū | D£® | ¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğÉĀĪ÷Ź”ø߶žÉĻŌĀæ¼Ņ»»Æѧ¾ķ£Ø½āĪö°ę£©£© ĢāŠĶ£ŗĢīæÕĢā
ĆŗµÄÖ±½ÓČ¼ÉÕ»į¶Ō“óĘųŌģ³ÉŃĻÖŲĪŪČ¾£¬ŹĒĪķö²ŠĪ³ÉµÄŅ»øöÖŲŅŖŌŅņ”£ŹµĻÖĆŗµÄĒå½ąĄūÓĆĘČŌŚĆ¼½Ž”£ŅŅ“¼”¢¼×“¼”¢ÄņĖŲµČ¾łÓėĆŗ»Æ¹¤Ļą¹Ų”£
¢ń£®£Ø1£©½«Ćŗ×Ŗ»Æ³ÉĖ®ĆŗĘųæÉÓŠŠ§ĢįøßÄÜŌ“ĄūÓĆĀŹ£ŗ
C(s)+H2O(g)  CO(g)£«H2(g) ¦¤H£½+131.3KJ/mol£¬·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK= ”£
CO(g)£«H2(g) ¦¤H£½+131.3KJ/mol£¬·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK= ”£
£Ø2£©Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚĢå»żæɱäµÄČŻĘ÷ÖŠĶ¶Čė·“Ó¦Īļ½ųŠŠ“Ė·“Ó¦£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®ĢåĻµÖŠ¼ÓČė“߻ƼĮ(ĘäĖūĢõ¼ž±£³Ö²»±ä)£¬Ę½ŗā²»ŅĘ¶Æµ«·“Ó¦µÄ¦¤H ½«±ä“ó
B£®ČōÕż”¢Äę·“Ó¦±ČÖµŗć¶Ø£¬ŌņĖµĆ÷Ę½ŗāŅŃ½ØĮ¢
C£®½ØĮ¢Ę½ŗāŗ󣬼ÓŃ¹£¬ĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮ潫Ōö“ó
D£®½ØĮ¢Ę½ŗāŗ󣬼ÓŃ¹£¬Ę½ŗāĻņÄę·½ĻņŅĘ¶Æ£¬Ę½ŗā³£Źż¼õŠ”
¢ņ£®ŅŅ“¼ŹĒÖŲŅŖµÄ»Æ¹¤²śĘ·ŗĶŅŗĢåČ¼ĮĻ£¬æÉŅŌĄūÓĆĻĀĮŠ·“Ó¦ÖĘČ”ŅŅ“¼”£
2CO2(g)+6H2(g)  CH3CH2OH(g)+3H2O(g) ¦¤H= a KJ/mol
CH3CH2OH(g)+3H2O(g) ¦¤H= a KJ/mol
ŌŚŅ»¶ØŃ¹ĒæĻĀ£¬²āµĆÉĻŹö·“Ó¦µÄŹµŃ鏿¾ŻČēĻĀ±ķ”£

øł¾Ż±ķÖŠŹż¾Ż·ÖĪö£ŗ
£Ø3£©ÉĻŹö·“Ó¦µÄa 0(Ģī”°>”±”°<”±»ņ”°=”±)
£Ø4£©ŌŚĪĀ¶ČĪŖT1Ź±£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżK=1£¬ŌŚ2LĆܱÕČŻĘ÷ÖŠ¼ÓČėŅ»¶ØĮæĢåĻµø÷ĪļÖŹ£¬·“Ó¦µÄijŹ±æĢ²āµĆ·“Ó¦ĢåĻµÖŠø÷ĘųĢå¾łĪŖ1mol”£
¢Ł“ĖŹ±V(CO2)Õż= V(CO2)Äę(Ģī”°>”±”°<”±»ņ”°=”±)
¢ŚČō·“Ó¦ŌŚŗćŃ¹¾ųČČČŻĘ÷ÖŠ½ųŠŠ£¬“ļĘ½ŗāŗó£¬CO2µÄĪļÖŹµÄĮæ
A£®“óÓŚ1mol B£®µČÓŚ1mol C£®Š”ÓŚ1mol D£®²»Č·¶Ø
¢ó£®CO2ŅąŹĒŗĻ³ÉÄņĖŲµÄÖŲŅŖŌĮĻ£¬ŅŌCO2ÓėNH3ĪŖŌĮĻŗĻ³ÉÄņĖŲ[»ÆѧŹ½ĪŖ[CO(NH2)2]µÄÖ÷ŅŖ·“Ó¦ČēĻĀ£¬ŅŃÖŖ£ŗ
¢Ł2NH3(g)+CO2(g)=NH2CO2 NH4(s) ¦¤H=+l59.5kJ”¤mol-1
¢ŚNH2CO2NH4(s) CO(NH2)2(s)+H2O(g) ¦¤H=+116.5kJ”¤mol-1
CO(NH2)2(s)+H2O(g) ¦¤H=+116.5kJ”¤mol-1
¢ŪH2O(l)=H2O(g) ¦¤H=+44.0kJ”¤mol-1
Š“³öCO2ÓėNH3ŗĻ³ÉÄņĖŲŗĶŅŗĢ¬Ė®µÄČČ»Æѧ·“Ó¦·½³ĢŹ½
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com