
【题目】将Na2O2和Na2O的混合物mg加入到过量的300g的水中完全反应后,产生标准状况下的气体224mL,在反应后的溶液中加入0. 5mol/L H2SO4溶液100mL,恰好中和至溶液呈中性,溶液的总体积为400mL,下列计算结果错误的是( )
A.m=3.42g
B.n( Na2O2) =0. 02mol
C.n(Na2O) : n(Na2O2) =3 :2
D.最后溶液中Na2SO4的浓度为0. 25mol/L
【答案】D
【解析】
A.Na2O2和Na2O的混合物与水反应方程式为:Na2O+H2O=2NaOH、2Na2O2+2H2O=4NaOH+O2↑,产生的气体为氧气,其物质的量为![]() =0.01mol,所以混合物中n(Na2O2)=0.02mol;加入硫酸溶液恰好中和至溶液呈中性时溶液中的溶质为Na2SO4,则有n(Na+)=2n(SO42-)=0.5mol/L×0.1L×2=0.1mol,根据元素守恒可知原混合物中n(Na2O)=
=0.01mol,所以混合物中n(Na2O2)=0.02mol;加入硫酸溶液恰好中和至溶液呈中性时溶液中的溶质为Na2SO4,则有n(Na+)=2n(SO42-)=0.5mol/L×0.1L×2=0.1mol,根据元素守恒可知原混合物中n(Na2O)=![]() =0.03mol;则混合物的质量m=0.03mol×62g/mol+0.02mol×78g/mol=3.42g,故A正确;
=0.03mol;则混合物的质量m=0.03mol×62g/mol+0.02mol×78g/mol=3.42g,故A正确;
B.根据A可知n(Na2O2)=0.02mol,故B正确;
C.n(Na2O) : n(Na2O2)=0.03mol:0.02mol=3:2,故C正确;
D.最后溶液中n(Na2SO4)=n(SO42-)=0.5mol/L×0.1L=0.05mol,所以浓度为![]() ,故D错误;
,故D错误;
故答案为D。


 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
【题目】H是一种香料,可用如图的设计方案合成。
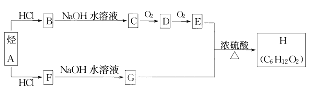
已知:①在一定条件下,有机物有下列转化关系:
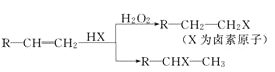
②烃A和等物质的量的HC1在不同的条件下发生加成反应,既可以生成只含有一个甲基的B,也可以生成含有两个甲基的F。
回答下列问题:
(1)D的结构简式为_______________________________________。
(2)烃A→B的化学反应方程式是____________________________________ 。
(3)F→G的化学反应类型为 _________________________________。
(4)E+G→H的化学反应方程式是 ____________________________________。
(5)H有多种同分异构体,其中含有一个羧基,且其烃基上一氯代物有两种的是 _____________(用结构简式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中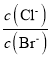 增大
增大
B.在0.1 mol/LCH3COONa溶液中:c(OH﹣)+0.1mol/L>c(CH3COOH)+c(H+)+c(Na+)
C.在10mL 0.1 mol/L的AgNO3溶液中加入6mL等浓度的NaCl溶液,有白色沉淀产生,再加入6 mL等浓度的Na2S溶液,溶液中又有黑色沉淀生成,说明Ksp(Ag2S)< Ksp(AgCl)
D.常温下,10 mL 0.02 mol/L HCl溶液与10 mL 0.02 mol/LBa(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A. 分子式为C8H8O2的芳香族化合物中属于羧酸的同分异构体有3种
B. 麦芽糖的水解产物有两种,且互为同分异构体
C. 等质量的苯和苯乙烯(![]() )完全燃烧,消耗氧气的体积相同
)完全燃烧,消耗氧气的体积相同
D. 分子式为C4H8Cl2且含有两个甲基的有机物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种医药中间体,可通过如图所示路线合成。A是石油化工的重要产品且分子中所有原子在同一平面内,H的分子式是C7H8。
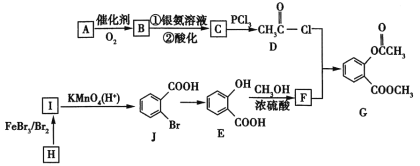
已知:![]() 。
。
回答下列问题。
(1)A的结构简式是___________。
(2)H→I的化学方程式为__________,B与银氨溶液反应的化学方程式是__________。
(3)C→D的反应类型是______,I→J的反应类型是______。
(4)两个E分子在一定条件下发生分子间脱水生成一种环状酯的结构简式是_______________。
(5)满足以下条件的F的同分异构体(不含F)共有_________种。
①能与氯化铁溶液发生显色反应 ②分子中有—COO—结构 ③苯环上有两个取代基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热某纯净的小苏打(NaHCO3)样品至固体质量不再变化,得到固体(Na2CO3)质量31.8g,将该固体溶于水配制成500mL溶液,计算:
(1)产生的气体冷却至标准状况下,其体积为多少升?______________
(2)求所得溶液中Na+的物质的量浓度?_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.现有下列仪器或用品:①铁架台(含铁圈、各式铁夹) ②锥形瓶 ③酸式滴定管和碱式滴定管 ④烧杯 ⑤玻璃棒 ⑥胶头滴管 ⑦天平(含砝码) ⑧滤纸 ⑨量筒 ⑩过滤漏斗;
现有下列药品:(A)NaOH固体 (B)标准NaOH溶液(C)未知浓度盐酸 (D)蒸馏水(E)碳酸钠溶液
根据所做过的学生实验,回答下列问题:
(1)过滤时,应选用的上述仪器是_________________________(填编号)。
(2)配制一定物质的量浓度的NaOH溶液时,还缺少的仪器是__________。
(3)做酸碱中和滴定时,还缺乏的试剂是____________________。
(4)进行中和滴定时,绝不可用将要盛的溶液事先润洗的仪器是下列的______(填编号)。甲.酸式滴定管 乙.碱式滴定管 丙.锥形瓶
(5)用标准的NaOH溶液滴定未知浓度的盐酸,选用酚酞作为指示剂,造成测定结果偏高的原因可能是______________。
A.配制标准溶液的NaOH中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
D.滴定前有气泡,滴定后气泡消失。
II. 甲醇(CH3OH)是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
反应II:CO(g)+2H2(g)![]() CH3OH(g) ΔH2
CH3OH(g) ΔH2
①反应I的平衡常数表达式为K=________________________
②下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH2______0,ΔS______0 (填“>”、“=”或“<”=)。
③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为________。
(2)已知在常温常压下,某实验小组依据甲醇燃烧的反应原理,设计如下图所示的电池装置:

①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH =-1275.6 kJ·mol-1
②H2O(g)=H2O(l) ΔH =-44.0 kJ·mol-1
①写出表示甲醇燃烧热的热化学方程式____________________。
②写出上图电池装置中负极反应式:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒乙酸是合成许多药用生物碱的重要中间体,以苯酚为原料制备胡椒乙酸的合成路线如图所示。

回答下列问题:
(1)下列关于有机物B的说法正确的是 ____________(填字母)。
a.能与FeCl3溶液发生显色反应
b.核磁共振氢谱中只有3组峰
c.能发生银镜反应
d.能与溴水发生加成反应
(2)C的名称是___________,C D的反应类型是_______。
(3)胡椒乙酸(E)中所含官能团的名称为 __________ 。
(4)G生成F的化学方程式为_____________。
(5)W是E的同分异构体,0.5 mol W与足量碳酸氢钠溶液反应生成1 mol C02,已知W的苯环上只有2个取代基,则W的结构共有__________(不含立体异构)种,其中核磁共振氢谱有五组峰的结构简式为_______。
(6)参照上述合成路线,写出以一氯甲苯(![]() )为原料(无机试剂任选)制备苯乙酸的合成路线:____________________
)为原料(无机试剂任选)制备苯乙酸的合成路线:____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物A~H的转换关系如下所示:
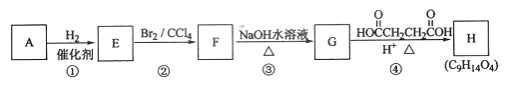
链烃A有支链且只有一个官能团,其相对分子质量在65~75之间,1 mol A完全燃烧消耗7 mol氧气,请回答下列问题:
(1)A的结构简式是________;
(2)由F转化为G的化学方程式是_______________________;
(3)G与金属钠反应能放出气体,由G转化为H的化学方程式是_______________;
(4)①的反应类型是___________;③的反应类型是____________;
(5)链烃B是A的同分异构体,分子中的所有碳原子共平面,其催化氢化产物为正戊烷,写出B任一可能的结构简式_______________________________;
(6)C也是A的一种同分异构体,它的一氯代物只有一种(不考虑立体异构,则C的结构简式为__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com