
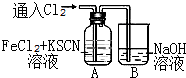 ¼×ѧɜ¶ŌCl2ÓėFeCl2ŗĶKSCN»ģŗĻČÜŅŗµÄ·“Ó¦½ųŠŠŹµŃéĢ½¾æ£®ĻņAÖŠĶØČėĀČĘųÖĮ¹żĮ棬·¢ĻÖAÖŠČÜŅŗĻČ³ŹŗģÉ«ŗóÖš½„±äĪŖ»ĘÉ«£®
¼×ѧɜ¶ŌCl2ÓėFeCl2ŗĶKSCN»ģŗĻČÜŅŗµÄ·“Ó¦½ųŠŠŹµŃéĢ½¾æ£®ĻņAÖŠĶØČėĀČĘųÖĮ¹żĮ棬·¢ĻÖAÖŠČÜŅŗĻČ³ŹŗģÉ«ŗóÖš½„±äĪŖ»ĘÉ«£®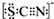 £®ŌņĢ¼ŌŖĖŲµÄ»ÆŗĻ¼ŪŹĒ+4
£®ŌņĢ¼ŌŖĖŲµÄ»ÆŗĻ¼ŪŹĒ+4·ÖĪö £Ø1£©CŌŖĖŲ·Ē½šŹōŠŌŠ”ÓŚS”¢NµÄ£¬¹²ÓƵē×Ó¶ŌĘ«ĻņS”¢NŌŖĖŲ£»
£Ø2£©Č”AÖŠ»ĘÉ«ČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČė×ćĮæµÄNaOHČÜŅŗ£¬ÓŠŗģŗÖÉ«³ĮµķÉś³É£¬Ó¦µ±ŹĒĒāŃõ»ÆĢś¹ĢĢ壬ĖłŅŌŌČÜŅŗÖŠÓ¦µ±ÓŠFe3+£¬¹żĀĖŗó½«ĀĖŅŗ·Ö³ÉĮ½·Ż£¬Ņ»·Ż¼ÓČėÓĆŃĪĖįĖį»ÆµÄBaCl2ČÜŅŗ£¬²śÉś°×É«³Įµķ£¬°×É«³ĮµķĪŖĮņĖį±µ£¬¼“ČÜŅŗÖŠÓŠSO42-Ąė×Ó£¬ĮķŅ»·Ż¼ÓČėÅØĮņĖįÖŠ£¬·ÅČėĶ·ŪŗóČÜŅŗ±äĄ¶²¢ÓŠĘųĢåÉś³É£¬ĘųĢåÓöæÕĘų±äŗģ×ŲÉ«£¬øĆŗģ×ŲÉ«ĘųĢåĪŖNO2£¬ĖµČÜŅŗÖŠÓŠNO3-£»
£Ø3£©SCN-ÓėCl2·“Ӧɜ³ÉSO42-”¢NO3-£¬Ģ¼ŌŖĖŲ²»Äܱ»Ńõ»Æ£¬ÓŠ¶žŃõ»ÆĢ¼Éś³É£¬ĖłŅŌĖüĆĒ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗSCN-+8Cl2+9H2O=NO3-+SO42-+CO2”ü+16Cl-+18H+£¬æÉŅŌ¼ĘĖć×ŖŅʵē×ÓŹżÄ棬ĒāŃõ»ÆÄĘČÜŅŗĪüŹÕ¶žŃõ»ÆĢ¼”¢Ī“·“Ó¦µÄĀČĘų£¬BÖŠĒāŃõ»ÆÄĘŹ£Óą£¬BÖŠČÜÖŹĪŖĢ¼ĖįÄĘ”¢ĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘÓėĒāŃõ»ÆÄĘ£®
½ā“š ½ā£ŗ£Ø1£©CŌŖĖŲ·Ē½šŹōŠŌŠ”ÓŚS”¢NµÄ£¬¹²ÓƵē×Ó¶ŌĘ«ĻņS”¢NŌŖĖŲ£¬ŌņSCN-ÖŠĢ¼ŌŖĖŲµÄ»ÆŗĻ¼ŪŹĒ+4¼Ū£¬
¹Ź“š°øĪŖ£ŗ+4£»
£Ø2£©Č”AÖŠ»ĘÉ«ČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČė×ćĮæµÄNaOHČÜŅŗ£¬ÓŠŗģŗÖÉ«³ĮµķÉś³É£¬Ó¦µ±ŹĒĒāŃõ»ÆĢś¹ĢĢ壬ĖłŅŌŌČÜŅŗÖŠÓ¦µ±ÓŠFe3+£¬¹żĀĖŗó½«ĀĖŅŗ·Ö³ÉĮ½·Ż£¬Ņ»·Ż¼ÓČėÓĆŃĪĖįĖį»ÆµÄBaCl2ČÜŅŗ£¬²śÉś°×É«³Įµķ£¬°×É«³ĮµķĪŖĮņĖį±µ£¬¼“ČÜŅŗÖŠÓŠSO42-Ąė×Ó£¬ĮķŅ»·Ż¼ÓČėÅØĮņĖįÖŠ£¬·ÅČėĶ·ŪŗóČÜŅŗ±äĄ¶²¢ÓŠĘųĢåÉś³É£¬ĘųĢåÓöæÕĘų±äŗģ×ŲÉ«£¬øĆŗģ×ŲÉ«ĘųĢåĪŖNO2£¬ĖµČÜŅŗÖŠÓŠNO3-£¬ČÜŅŗ±äĄ¶µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ3Cu+2NO3-+8H+=2NO”ü+3Cu2++4H2O£¬
¹Ź“š°øĪŖ£ŗFe3+£»SO42-£»3Cu+2NO3-+8H+=2NO”ü+3Cu2++4H2O£»
£Ø3£©SCN-ÓėCl2·“Ӧɜ³ÉSO42-”¢NO3-£¬Ģ¼ŌŖĖŲ²»Äܱ»Ńõ»Æ£¬ÓŠ¶žŃõ»ÆĢ¼Éś³É£¬ĖłŅŌĖüĆĒ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗSCN-+8Cl2+9H2O=NO3-+SO42-+CO2”ü+16Cl-+18H+£¬“Ė·“Ó¦ÖŠµē×Ó×ŖŅĘŹżÄæĪŖ16£¬¼“ÓÉ·½³ĢŹ½æÉÖŖĆæÉś³É1mol¶žŃõ»ÆĢ¼ŅŖ×ŖŅĘ16molµē×Ó£®ĒāŃõ»ÆÄĘČÜŅŗĪüŹÕ¶žŃõ»ÆĢ¼”¢Ī“·“Ó¦µÄĀČĘų£¬BÖŠĒāŃõ»ÆÄĘŹ£Óą£¬BÖŠČÜÖŹĪŖĢ¼ĖįÄĘ”¢ĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘÓėĒāŃõ»ÆÄĘ£¬ČÜŅŗÖŠµÄŅõĄė×ÓÓŠOH-ŗĶCl-”¢ClO-”¢CO32-”¢HCO3-£¬
¹Ź“š°øĪŖ£ŗ16£»Cl-”¢ClO-”¢CO32-”¢HCO3-£®
µćĘĄ ±¾ĢāŹĒĢ½¾æŹµŃé·½°øµÄ×ŪŗĻĢā£¬²ąÖŲæ¼²éѧɜ·ÖĪöĶĘĄķÄÜĮ¦£¬ŅŖŹģĮ·ÕĘĪÕŌŖĖŲ»ÆŗĻĪļŠŌÖŹ£¬£Ø3£©ÖŠµē×Ó×ŖŅĘĪŖŅדķµć£¬ĄūÓĆ·½³ĢŹ½½įŗĻĀČŌŖĖŲ»ÆŗĻ¼Ū±ä»Æ¼ĘĖć£¬±ÜĆāS”¢NŌŖĖŲ»ÆŗĻ¼ŪÅŠ¶Ļ£¬øł¾Żµē×ÓŹ½æÉÖŖSCN-ÖŠNĪŖ-3¼Ū”¢SĪŖ-2¼Ū£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
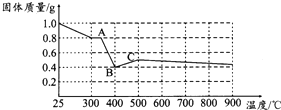 ²ŻĖįŃĒĢś¾§Ģå£ØFeC2O4•2H2O£©³Źµ»ĘÉ«£®Ä³æĪĢā×éĪŖĢ½¾æ²ŻĖįŅµĢś¾§ĢåµÄ»ÆѧŠŌÖŹ£¬½ųŠŠĮĖŅ»ĻµĮŠŹµŃéĢ½¾æ£®
²ŻĖįŃĒĢś¾§Ģå£ØFeC2O4•2H2O£©³Źµ»ĘÉ«£®Ä³æĪĢā×éĪŖĢ½¾æ²ŻĖįŅµĢś¾§ĢåµÄ»ÆѧŠŌÖŹ£¬½ųŠŠĮĖŅ»ĻµĮŠŹµŃéĢ½¾æ£®| ŹµŃé²½Öč£Ø²»ŅŖĒ󊓳ö¾ßĢå²Ł×÷¹ż³Ģ£© | Ō¤ĘŚŹµŃéĻÖĻóŗĶ½įĀŪ |
| ȔɣĮæŗŚÉ«¹ĢĢ壬¼ÓČėŹŹĮæĻ”ŃĪĖį£Ø»ņĻ”ĮņĖį£©Čܽā£¬ŌŚČÜŅŗÖŠ¼ÓČėKSCNČÜŅŗ | ČōČÜŅŗ²»±äŗģÉ«£¬Ōņ¼ŁÉčŅ»³ÉĮ¢£»ČōČÜŅŗ±äŗģÉ«£¬Ōņ¼ŁÉčŅ»²»³ÉĮ¢ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ¢Ł | ¢Ś | ¢Ū | ¢Ü | |
| X | NaOHČÜŅŗ | KOHČÜŅŗ | O2 | FeCl3ČÜŅŗ |
| Y | Al£ØOH£©3 | SiO2 | N2 | Cu |
| Z | Ļ”ĮņĖį | ÅØŃĪĖį | H2 | ÅØĻõĖį |
| A£® | ¢Ł¢Ū | B£® | ¢Ł¢Ü | C£® | ¢Ś¢Ü | D£® | ¢Ś¢Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ³ĮµķĪļ | Al£ØOH£©3 | Fe£ØOH£©3 | Fe£ØOH£©2 | Mn£ØOH£©2 | Cu£ØOH£©2 | Zn£ØOH£©2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ”Ż-0.42 | ”Ż2.5 | ”Ż7 | ”Ż7 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬78g Na2O2ŗ¬ÓŠµÄŅõĄė×ÓŹżĪŖNA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬22.4 LĒāĘųÖŠŗ¬ĒāŌ×ÓŹżÄæĪŖ2 NA | |
| C£® | 0.5 mol/LµÄNaClČÜŅŗÖŠ£¬ŗ¬ÓŠCl-ŹżÄæĪŖ0.5 NA | |
| D£® | 1mol FeŌŚ×ćĮæĀČĘųÖŠĶźČ«·“Ó¦£¬Ź§Č„µÄµē×ÓŹżĪŖ2 NA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com