
用pH试纸测溶液的pH时应注意什么问题?记录数据时又要注意什么?是否可用pH试纸测定氯水的pH?
 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中箭头表示溶液中阴离子移动的方向。下列说法不正确的是( )
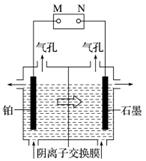
A.M是电源的负极
B.左侧气孔逸出的气体可能为副产物H2
C.电解槽中发生的总反应为MnSO4+2H2O MnO2+H2↑+H2SO4
MnO2+H2↑+H2SO4
D.若用阳离子交换膜代替阴离子交换膜,阳极可能得到MnO2
查看答案和解析>>
科目:高中化学 来源: 题型:
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知:CH4(g)+H2O(g)===CO(g)+3H2(g)
ΔH=206.2 kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g)
ΔH=247.4 kJ·mol-1
2H2S(g)===2H2(g)+S2(g)
ΔH=169.8 kJ·mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为________________________________________________________________________。
(2)H2S热分解制氢时,常向反应器中通入一定比例空气,使部分H2S燃烧,其目的是____________________________;燃烧生成的SO2与H2S进一步反应,生成物在常温下均非气体,写出该反应的化学方程式:_____________________________________________。
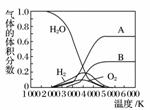
(3)H2O的热分解也可得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如下图所示。图中A、B表示的物质依次是________________________。
(5)Mg2Cu是一种储氢合金。350 ℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077)。Mg2Cu与H2反应的化学方程式为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同
B.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH相同
C.已知:①2H2(g)+O2(g)===2H2O(g) ΔH1=-a kJ·mol-1,②2H2(g)+O2(g)===2H2O(l)
ΔH2=-b kJ·mol-1,则a>b
D.已知:①C(石墨,s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1,②C(金刚石,s)+O2(g)===
CO2(g) ΔH2=-395.0 kJ·mol-1,则金刚石比石墨稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,相同物质的量浓度的下列溶液:①NaCl ②NaOH ③H2SO4 ④(NH4)2SO4,其中水的电离程度按由大到小顺序排列的一组是( )
A.④>③>②>① B.②>③>①>④
C.④>①>②>③ D.③>②>①>④
查看答案和解析>>
科目:高中化学 来源: 题型:
在某温度时,测得0.01 mol·L-1的NaOH溶液的pH=11。
(1)该温度下水的离子积常数Kw=______________。
(2)在此温度下,将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合。
①若所得混合液为中性,且a=12,b=2,则Va∶Vb=_____________。
②若所得混合液为中性,且a+b=12,则Va∶Vb=__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视________,直到因加入一滴盐酸后,溶液由黄色变为橙色,并______为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是________(填字母序号)。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为________mL,终点读数为________mL,
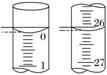
所用盐酸溶液的体积为________mL。
(4)某学生根据3次实验分别记录有关数据如下表:
| 滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据上表数据列式计算该NaOH溶液的物质的量浓度。
答案 (1)锥形瓶中溶液颜色变化 在半分钟内不变色
(2)D (3)0.00 26.10 26.10
(4) =
=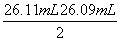 =26.10 mL,c(NaOH)=
=26.10 mL,c(NaOH)=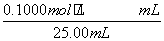 =0.104 4 mol·L-1
=0.104 4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL未知浓度的盐酸(酚酞作指示剂)的滴定曲线如图所示。下列说法正确的是( )
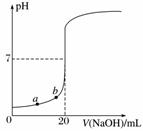
A.水电离出的氢离子浓度:a>b
B.盐酸的物质的量浓度为0.010 0 mol·L-1
C.指示剂变色时,说明盐酸与NaOH恰好完全反应
D.当滴加NaOH溶液10.00 mL时(忽略反应前后体积变化),该混合液的pH=1+lg 3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com