
| A.-Y kJ/mol | B.-(10X-Y) kJ/mol |
| C.-(5X-0.5Y) kJ/mol | D.+(10X-Y) kJ/mol |
科目:高中化学 来源:不详 题型:单选题
| A.SO2的催化氧化反应是吸热反应 |
| B.SO2的转化率一定为20% |
| C.导出气体中SO3所占的体积分数为2 / 9 |
| D.单位时间内进入接触室的气体与从接触室导出的气体的物质的量之比为9∶10 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2c(g),△H<0;达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是
2c(g),△H<0;达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是| | X | Y |
| A | 再加入B | B的转化率 |
| B | 再加入C | A的体积分数 |
| C | 增大压强 | A的转化率 |
| D | 升高温度 | 混合气体平均摩尔质量 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
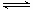 2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:| A.①③ | B.①④ | C.②③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
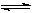 CH3OH(g) + H2O(g) △H=" -49.0" kJ·mol-1
CH3OH(g) + H2O(g) △H=" -49.0" kJ·mol-1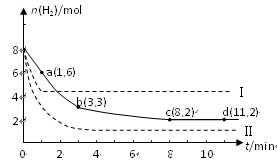
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
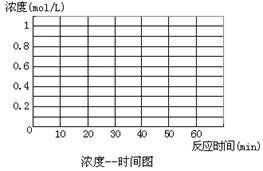
 B + D在不同条件下进行,B、D的起始浓度为0,把反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示。
B + D在不同条件下进行,B、D的起始浓度为0,把反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示。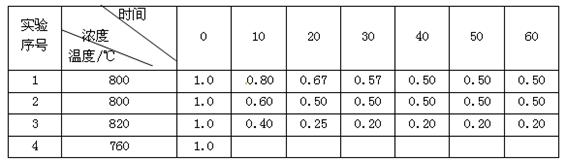
 www.k@s@5
www.k@s@5 @u.com
@u.com 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com