
| A. | 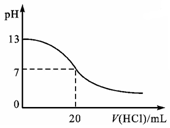 表示V L 0.1mol/L的氨水中滴加某种浓度的盐酸时,溶液pH的变化情况 | |
| B. | 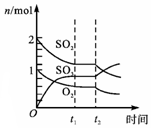 表示SO2与O2的可逆反应,t2时刻条件的改变可能是压强 | |
| C. | 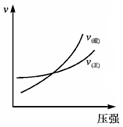 表示一个气体总休积减小的可逆反应中,压强与反应速率的关系 | |
| D. | 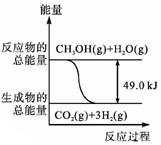 表示某种放热反应,反应热为49.0kJ |
分析 A.酸碱中和反应滴定过程中溶液PH出现突越;
B.浓度在原来浓度基础上二氧化硫和氧气浓度减小,三氧化硫浓度增大;
C.正反应为气体体积减小的反应,增大压强平衡正向进行;
D.反应热单位为KJ/mol.
解答 解:A.V L 0.1mol/L的氨水中滴加某种浓度的盐酸时,溶液呈中性时体积不一定为20ml,变化过程中接近反应终点溶液pH的变化出现突越,图象不符合,故A错误;
B.SO2与O2的可逆反应,是气体体积减小的放热反应,t2时刻条件的改变使得二氧化硫和氧气浓度减小,三氧化硫浓度增大,则可能是增大体积减小压强,改变条件可能是压强,故B正确;
C.气体总休积减小的可逆反应中,压强增大平衡正向进行,正反应速率大于逆反应速率,故C错误;
D.反应热△H=-49.0kJ/mol,故D错误;
故选B.
点评 本题考查了弱电解质电离平衡、化学平衡影响因素、反应热的分析判断、掌握化学平衡影响原理和反应热概念是解题关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 相同温度下,CuS的溶解度小于ZnS的溶解度 | |
| B. | 除去工业废水中的Fe2+,可以选用CuS做沉淀剂 | |
| C. | 足量CuSO4溶解在0.1mol/L的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol/L | |
| D. | 在ZnS的饱和溶液中,加入FeCl2溶液,一定不产生FeS沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 95%的酒精用于医疗中可作消毒剂,硫酸钡用于医疗中可作钡餐 | |
| B. | 食品中用木糖醇作甜味剂,可降低糖尿病的犯病几率 | |
| C. | 焊接废旧钢材前,分别用饱和Na2CO3溶液、NH4Cl溶液处理焊点 | |
| D. | 钙基固硫和NOx的催化转化都是解决空气污染问题的措施 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL4mol/L的硫酸与足量Cu共热,转移的电子数为0.4NA | |
| B. | 1L 0.1mol•L-1的Na2CO3溶液中含有阳离子的总数为0.2NA | |
| C. | O2和O3的混合物共3.2g,其中所含氧原子数一定为0.2NA | |
| D. | 室温时,pH=12的Ba(OH)2溶液中,氢氧根离子数目为10-2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用灼烧的方法可以区分羊毛和人造纤维 | |
| B. | 医用消毒酒精是体积分数为95%的乙醇 | |
| C. | 食用一定量的油脂能促进人体对某些维生素的吸收 | |
| D. | 加热能杀死流感病毒是因为蛋白质受热变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将气体通入AgNO3溶液 | B. | 将气体通过干燥的有色布条 | ||
| C. | 将气体通过干燥的红色石蕊试纸 | D. | 将气体通入含有KSCN的FeCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4L NO和11.2L O2在密闭容器中充分反应后,总分子数小于NA | |
| B. | 28g C2H4和C3H6的混合物含有C-H键数目为4NA | |
| C. | 标准状况下,22.4L Cl2与适量H2O或NaOH反应转移的电子数目都为NA | |
| D. | 常温下,1L pH=13的Ba(OH)2中OH-的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的化学方程式为:CO2+H2 $?_{高温}^{催化剂}$ CO+H2O | |
| B. | 恒温恒容下,增大压强,H2 浓度一定减小 | |
| C. | 升高温度,逆反应速率减小 | |
| D. | 该反应的反应热为负值 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com