
 (1)由于SiH4具有易提纯的特点,因此硅烷热分解法是制备高纯硅很有发展潜力的方法.制备硅烷整个过程必须严格控制无水,否则生成的硅烷将发生变质,其化学方程式为SiH4+3H2O=4H2+H2SiO3,整个系统还必须与氧隔绝,其原因是SiH4+O2=SiO2+2H2O(用化学方程式表示)
(1)由于SiH4具有易提纯的特点,因此硅烷热分解法是制备高纯硅很有发展潜力的方法.制备硅烷整个过程必须严格控制无水,否则生成的硅烷将发生变质,其化学方程式为SiH4+3H2O=4H2+H2SiO3,整个系统还必须与氧隔绝,其原因是SiH4+O2=SiO2+2H2O(用化学方程式表示)分析 (1)硅烷与水反应生成氢气和硅酸;硅烷不稳定容易被空气中的氧气氧生成二氧化硅和水;
(2)分析反应中元素化合价变化,所含元素化合价降低反应物为氧化剂;
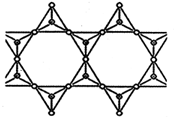
(3)根据价层电子对互斥理论判断原子杂化方式;根据图中的一个结构单元中含有1个硅、3个氧原子,化学式为SiO32-.
解答 解:(1)硅烷与水反应生成氢气和硅酸,化学方程式:SiH4+3H2O=4H2+H2SiO3;硅烷不稳定容易被空气中的氧气氧生成二氧化硅和水,化学方程式:SiH4+O2=SiO2+2H2O;
故答案为:SiH4+3H2O=4H2+H2SiO3;SiH4+O2=SiO2+2H2O;
(2)3SiO2+6C+2N2$\frac{\underline{\;高温\;}}{\;}$Si3N4+6CO,反应中氮气中0价的氮元素化合价降为-3价,所以氮气为氧化剂;
故答案为:N2;
(3)该离子中每个Si原子价层电子对个数都是4,所以Si原子采用sp3杂化,故答案为:sp3;
根据图中的一个小的结构单元中含有1个硅,2个氧原子属于该结构,还有2个与其它结构单元共用,则O原子数为2+2×$\frac{1}{2}$=3,所以化学式为SiO32-;
故答案为:sp3;SiO32-.
点评 本题考查了化学方程式的书写,杂化类型的判断,物质结构图的分析应用,明确硅及其化合物的结构及性质是解题关键,题目难度较大.


科目:高中化学 来源: 题型:选择题
| A. | N4与N2互为同位素 | |
| B. | N4H44+与NaOH溶液反应的离子方程式为N4H44++4OH-═N4+4H2O | |
| C. | N4H4(SO4)2为弱电解质 | |
| D. | N4H44+中只含有极性共价键,不含非极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丁烷的结构简式为CH3CH2CH2CH3 | B. | 一氯乙烷的结构式为CH3Cl | ||
| C. | 四氯化碳的电子式为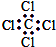 | D. | 苯的分子式为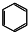 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
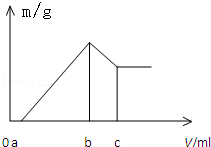 将镁、铝的混合物0.1mol 溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L 的NaOH溶液,沉淀质量m 随加入NaOH溶液的体积V 变化情况如图所示,计算:
将镁、铝的混合物0.1mol 溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L 的NaOH溶液,沉淀质量m 随加入NaOH溶液的体积V 变化情况如图所示,计算:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
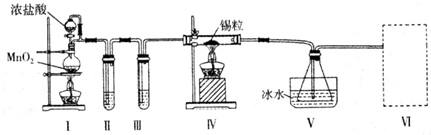
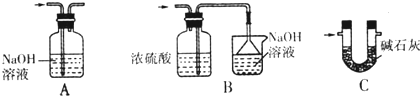
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 27g铝与足量的盐酸或NaOH溶液反应,转移电子的数目均为3NA | |
| B. | 1mol的羟基与1mol的氢氧根离子所含电子数均为10NA | |
| C. | 22.4 L氨气中含有N-H键的个数为3NA | |
| D. | Fe与水蒸气在高温条件下反应,有1mol Fe参与反应,则转移电子的数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 资料卡片 | ||
| 物质 | 熔点 | 沸点 |
| SiCl4 | -70℃ | 57.6℃ |
| TiCl4 | -25℃ | 136.5℃ |
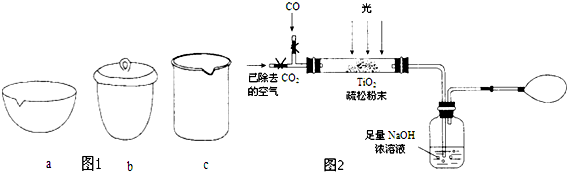
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数为55 | B. | 电子数是55 | C. | 中子数是137 | D. | 质量数是137 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com