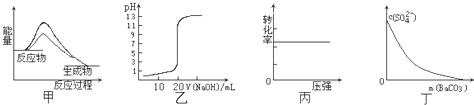
某温度下,反应H
2(g)+I
2(g)?2HI(g),在带有活塞的密闭容器中进行.
(1)已知:断开1mol H-H键要吸收436kJ的能量,断开1mol I-I键要吸收151kJ的能量,断开1mol H-I键要吸收299kJ的能量.则上述反应是
反应.(填“放热”或“吸热”)
(2)下列说法中正确的是:
A.温度、压强均不变,充入HI气体瞬间正反应速率增大
B.容器体积不变,升温逆反应速率增大
C.容器体积、温度不变,充入氦气后,正反应速率将增大
D.恒温恒容时,混合气体的平均分子量不变不能作为达平衡的标志
(3)若在体积为5L的容器中,起始时投入3mol H
2、2mol I
2,lOs达平衡时测得HI的物质的量为1.2mol.lOs内用H
2表示的平均反应速率为
,达平衡时I
2的转化率为
.
(4)若反应过程中某一时刻H
2、I
2、HI的浓度分别为0.3mol?L
-1、0.2mol?L
-l、0.4mol?L1
-1.当反应达到限度时,可能存在的数据是:
A.H
2为 0.5mol.L
-1,I
2为 0.4mol?L
-1B.H
2为 0.4mol?L
-1C.H
2、HI均为0.2mol?L
-1D.HI为 0.8mol?L
-1.



 作业辅导系列答案
作业辅导系列答案