
【题目】把3molP和2.5molQ置于2L密闭容器中,发生如下反应:3P(g)+Q(g)x M(g)+2N(g),5min后达到平衡生成1molN,经测定M的平均速率是0.1mol/(Lmin),下列叙述不正确的是( )
A.P的平均反应速率为0.15 mol/(Lmin)
B.Q的平衡浓度为1 mol/L
C.Q的转化率为25%
D.x等于2
【答案】C
【解析】解:A.已知达到平衡生成1molN,则参加反应的P为n(P)= ![]() ×1mol=1.5mol,所以v(P)=
×1mol=1.5mol,所以v(P)= ![]() =
= ![]() =0.15 mol/(Lmin),故A正确; B.已知达到平衡生成1molN,则参加反应的Q为n(Q)=
=0.15 mol/(Lmin),故A正确; B.已知达到平衡生成1molN,则参加反应的Q为n(Q)= ![]() n(N)=0.5mol,所以Q的平衡浓度为:
n(N)=0.5mol,所以Q的平衡浓度为: ![]() =1 mol/L,故B正确;
=1 mol/L,故B正确;
C.参加反应的Q为n(Q)= ![]() n(N)=0.5mol,故Q的转化率为
n(N)=0.5mol,故Q的转化率为 ![]() ×100%=20%,故C错误;
×100%=20%,故C错误;
D.根据A选项可知v(P)=0.15 mol/(Lmin),而M的平均速率是0.1mol/(Lmin),根据速率之比等于化学计量数之比,则 ![]() =
= ![]() ,所以x=2,故D正确;
,所以x=2,故D正确;
故选C.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】PbI2是生产新型敏化太阳能电池的敏化剂﹣﹣甲胺铅碘的原料.合成PbI2的实验流程如图1: 
(1)将铅块制成铅花的目的是 .
(2)31.05g铅花用5.00molL﹣1的硝酸溶解,至少需消耗5.00molL﹣1硝酸mL,同时产生L(标准状况下)NO.
(3)取一定质量(CH3COO)2PbnH2O样品在N2气氛中加热,测得样品固体残留率( ![]() ×100%)随温度的变化如图2所示(已知:样品在75℃时已完全失去结晶水).
×100%)随温度的变化如图2所示(已知:样品在75℃时已完全失去结晶水).
①(CH3COO)2PbnH2O中结晶水数目n=(填数字).
②100~200℃间分解产物为铅的氧化物和一种有机物,则该有机物为(写结构简式).
(4)称取一定质量的PbI2固体,用蒸馏水配制成室温时的饱和溶液,准确移取25.00mLPbI2饱和溶液分次加入阳离子交换树脂RH中,发生:2RH(s)+Pb2+(aq)=R2Pb(s)+2H+(aq),用锥形瓶接收流出液,最后用蒸馏水淋洗树脂至流出液呈中性,将洗涤液合并到锥形瓶中.加入2~3滴酚酞溶液,用0.002500molL﹣1NaOH溶液滴定,到滴定终点时用去氢氧化钠标准溶液20.00mL.计算室温时PbI2 的Ksp (请给出计算过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(反应中部分物质已略去)。A、C、G、K、M 为单质,其中G、K、L、M 为气体,其中M能使带火星的木条复燃,D可用作耐高温材料,B为黑色磁性氧化物, E为常见的强碱。

(1)D的化学式为__。
(2)写出反应①的离子方程式:__。
(3)写出反应②的离子方程式:__。
(4)写出反应③的化学方程式,并用单线桥表示电子转移的方向和数目:__。
【答案】 Al2O3 2Al+2OH—+2H2O=2AlO![]() +3H2↑ 2Fe2++Cl2=2Fe3++2Cl-
+3H2↑ 2Fe2++Cl2=2Fe3++2Cl- ![]()
【解析】M为气体单质,且M能使带火星的木条复燃,则M为O2;D可作耐高温材料,则D可能为高熔点的Al2O3或MgO;B为黑色磁性氧化物,则B为Fe3O4。“A+B→C+D”,A、C为单质,B、D为金属氧化物,则该反应为高温条件下金属间的置换反应,则A、C为金属单质,B为Fe3O4,可知C为Fe;E为强碱,A为金属单质,A与E反应生成气体单质G,所以A为两性金属Al,D为Al2O3,G为H2。“G+K→L”,G为H2,K为气体单质,L+B(Fe3O4)→F+H,又“F+E(强碱)→I”,则可推测F中含有铁的阳离子,与强碱反应生成沉淀;逆推L应为酸,两种单质化合得到的酸,则K为Cl2,L为HCl;Fe3O4溶于盐酸生成FeCl2和FeCl3;根据F+K(Cl2)→H,可得F为FeCl2,H为FeCl3;沉淀I+M(O2)→J,则沉淀I为Fe(OH)2,J为Fe(OH)3。
(1)根据上述分析,D为Al2O3;
(2)反应①为Al与强碱反应生成AlO2-和H2,离子方程式为2Al+2OH—+2H2O=2AlO2-+3H2↑;
(3)反应②为FeCl2+ Cl2→FeCl3,离子方程式为2Fe2++Cl2=2Fe3++2Cl-;
(4)反应③为Fe(OH)2被氧气氧化为Fe(OH)3,反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3;其中4mol Fe(OH)2失去4mol电子,氧气得电子,故单线桥可表示为:![]() 。
。
【题型】推断题
【结束】
24
【题目】海带中提取碘的一种流程如下:
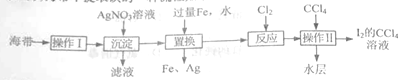
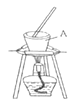
(1) “操作Ⅰ”的主要目的的是获得含I-的溶液,它包括灼烧、水浸。其中灼烧时装置如右图所示,仪器A的名称为__。
(2)“置换”所得滤渣中含有Fe和Ag。
①使用化学方法分离出Ag操作是__。
②分离出的Ag用稀硝酸转化为AgNO3,以循环利用,相关离子方程式为__。
(3)“操作Ⅱ”得到水层的方法是:将通入Cl2后的溶液置于分液漏斗中,加入CC14,振荡静置,__。
(4)检验“操作Ⅱ”所得水层中是否含有Fe3+的方法是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定碱式碳酸钴[COx(OH)y(CO3)z]的化学组成,研究性学习小组的同学设计了如图所示的装置进行实验探究.已知:碱式碳酸钴受热时可分解生成三种氧化物. 
(1)按如图所示装置组装好仪器,并;称取3.65g样品置于硬质玻璃管内,加热,当乙装置中(填实验现象),停止加热;打开活塞a,缓缓通入空气数分钟,通入空气的目的是 .
(2)某同学认为上述实验中存在一个缺陷,该缺陷是 .
(3)通过正确实验测得乙、丙装置增重分别为0.36g、0.88g,则该碱式碳酸钴的化学式为 .
(4)CoCl26H2O常用作多彩水泥的添加剂.以含钴废料(含少量Fe、Al等杂质)制取COCl26H2O的一种工艺如下: 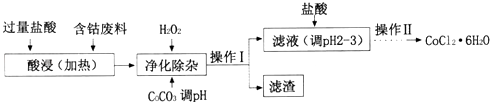
已知;25℃时
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
①净化除杂时,加入H2O2发生反应的离子方程式为;
②加入CoCO3调pH为5.2~7.6,则操作I获得的滤渣成分为;
③加盐酸调整pH为2~3的目的为;
④操作Ⅱ过程为蒸发浓缩、冷却结晶、过滤.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于反应:mA(g)+nB(g)cC(g)+dD(g),C物质的质量分数(C%)与温度、压强的关系如图所示,下列判断正确的是( ) 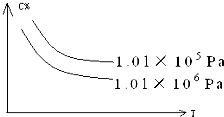
A.△H<0△S>0
B.△H>0△S<0
C.△H>0△S>0
D.△H<0△S<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时某些弱酸的电离平衡常数如下表所示:
CH3COOH | HClO | H2CO3 |
K(CH3COOH) | K(HClO) | K(H2CO3)a1=4.4×10﹣7 |
常温下,稀释CH3COOH、HClO两种酸时,溶液的pH随加水量变化的曲线如图所示,下列说法正确的是( )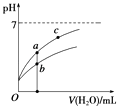
A.相同浓度的CH3COOH和HClO的混合溶液中,各离子浓度的大小关系是:c(H+)>c(ClO﹣)>c(CH3COO﹣)>c(OH﹣)
B.图象中a、c两点所处的溶液中 ![]() 相等(HR代表CH3COOH或HClO)
相等(HR代表CH3COOH或HClO)
C.图象中a点酸的浓度大于b点酸的浓度
D.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO﹣+CO2+H2O=2HClO+CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaHCO3和 KHCO3的混合物6.2g与100mL 盐酸恰好完全反应,得到标准状况下CO2的体积为1.568L.求:
(1)混合物中NaHCO3的质量是多少?
(2)盐酸的物质的量的浓度是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应: CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=;
(2)该反应为反应(选填吸热、放热);
(3)某温度下,平衡浓度符合下式:3c(CO2)c(H2)=5c(CO)c(H2O),试判断此时的温度为℃;
(4)830℃时,向该容器中加入1L CO2与1L H2 , 平衡时CO2的体积分数是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com