
| A. | 将苯加入溴水中振荡后,水层接近无色,是因为发生了取代反应 | |
| B. | 1 体积某气态烃与 HC1 充分加成消耗 HC11体积,加成后的物质最多还能和 5 体 积氯气发生取代反应,由此推断原气态烃是乙烯 | |
| C. | 乙醇与钠、氢氧化钠溶液均反应 | |
| D. | 等质量的乙烯和乙醇在氧气中充分燃烧后耗氧量相同. |
分析 A.苯与溴水不反应;
B.与HCl以1:1加成,含双键,且加成后的物质最多还能和 5 体 积氯气发生取代反应,则加成产物含5个H;
C.乙醇含-OH,与Na反应生成氢气;
D.1mol乙烯和乙醇在氧气中充分燃烧均消耗3mol氧气,等质量时二者的物质的量不同.
解答 解:A.苯与溴水不反,发生萃取,故A错误应;
B.与HCl以1:1加成,含双键,且加成后的物质最多还能和 5 体 积氯气发生取代反应,则加成产物含5个H,则原气态烃是乙烯,故B正确;
C.乙醇含-OH,与Na反应生成氢气,与NaOH不反应,故C错误;
D.1mol乙烯和乙醇在氧气中充分燃烧均消耗3mol氧气,等质量时二者的物质的量不同,则消耗的氧气不同,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机反应的判断,题目难度不大.


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁与盐酸反应:H++OH-═H2O | |
| B. | 铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氧化铜溶于稀硫酸:CuO+2H+═Cu2++H2O | |
| D. | 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2+H2O→H2SO3 | B. | Cl2+H2O→HCl+HClO | ||
| C. | 2F2+2H2O→4HF+O2 | D. | 2Na+2H2O→2NaOH+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  过滤时,应将漏斗颈尖嘴处紧贴烧杯内壁 | |
| B. |  蒸发时,当溶液完全蒸干时应立即停止加热 | |
| C. |  蒸馏时,应将开始馏出的部分液体弃去 | |
| D. |  分液时,当下层液体刚好放完时应立即关闭活塞,以免上层液体流出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 使紫色石蕊试液变红 | B. | 易溶于水 | ||
| C. | 发生酯化反应 | D. | 无色无味 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 四氧化三锰(Mn3O4)在电子工业有广泛应用.
四氧化三锰(Mn3O4)在电子工业有广泛应用.| 序号 | 反应 | △H(kJ•mol-1) | K | |
| 300°C | 800°C | |||
| Ⅰ | MnCO3(s)+$\frac{1}{2}$O2(g)?MnO2(s)+CO2(g) | a | 3.0×107 | 1.8×105 |
| Ⅱ | MnCO3(s)+$\frac{1}{4}$O2(g)?$\frac{1}{2}$Mn2O3(s)+CO2(g) | b | 1.7×103 | 2.4×105 |
| Ⅲ | MnCO3(s)+$\frac{1}{6}$O2(g)?$\frac{1}{3}$Mn3O4(s)+CO2(g) | c | 9.8 | 9.6×104 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
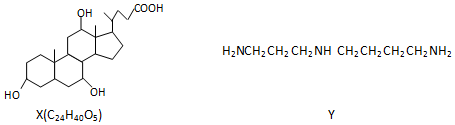
| A. | 1molX在浓硫酸作用下发生消去反应,最多生成3molH2O | |
| B. | 1molY发生类似酯化的反应,最多消耗2molX | |
| C. | X与足量HBr反应,所得有机物的分子式为C24H37O2Br3 | |
| D. | Y与癸烷的分子链均呈锯齿形,但Y的极性较强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com