
| A. | 食盐的溶解 | B. | 硬脂酸钠的盐析 | C. | CuCl2的水解 | D. | 蛋白质的变性 |
分析 A.食盐加水溶解,蒸发可得固体食盐;
B.硬脂酸钠的盐析溶解度减小析出,加入水会继续溶解;
C.盐类的水解比较微弱,存在水解平衡,是可逆过程;
D.蛋白质变性是在某些物理因素和化学因素影响下,蛋白质失去原有的生理活性.
解答 解:A.食盐加水溶解,蒸发食盐析出,因此食盐的溶解是可逆的过程,故A错误;
B.硬脂酸钠的盐析溶解度减小析出,加入水会继续溶解,因此是一个可逆过程,故B错误;
C.CuCl2的水解比较微弱,存在水解平衡,是一个可逆过程,故C错误;
D.蛋白质变性是在某些物理因素和化学因素影响下,蛋白质的理化性质和生理功能发生改变的现象,是一个不可逆过程,故D正确;
故选D.
点评 本题考查了可逆反应的特征分析应用,主要是理解物质性质的分析判断,掌握基础是关键,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃烧产物只有CO2和H2O | B. | 与溴水发生取代反应 | ||
| C. | 都难溶于水 | D. | 通常不与强酸、强碱、强氧化剂反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 540 mL | B. | 336 mL | C. | 224 mL | D. | 168 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
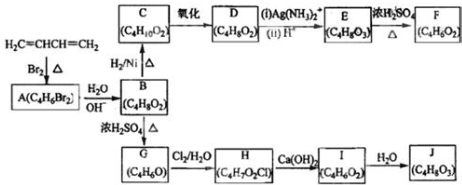
 ;
; +H2O,E中的官能团有羟基、羧基(填名称),与E具有相同官能团的E的同分异构体还有
+H2O,E中的官能团有羟基、羧基(填名称),与E具有相同官能团的E的同分异构体还有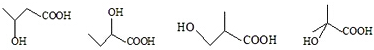 (写出结构简式,不考虑立体结构);
(写出结构简式,不考虑立体结构);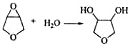 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.6g | B. | 1.8g | C. | 7.2g | D. | 4.8g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
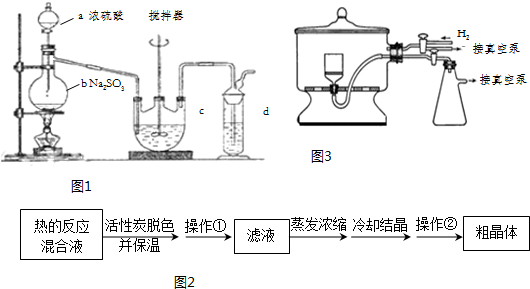
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验事实 | 结论 | |
| A | A元素的原子半径比B元素的原子半径大 | 周期表中A位于B的下一周期 |
| B | 将CO2通入到Na2SiO3溶液中产生白色浑浊 | 酸性:H2CO3>H2SiO3 |
| C | 常温下,铜能与浓硝酸反应而铝被浓硝酸钝化 | 还原性:Cu>Al |
| D | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com