
| 营养液所含成分 | 质量(g) |
| KCl | a |
| K2SO | b |
| NH4Cl | 428 |
| A. | 53.5 和214 | B. | 74.5 和348 | C. | 74.5 和696 | D. | 149 和696 |
分析 由428gNH4Cl可计算其物质的量,再由NH4Cl、K2SO4、KCl三种固体原料的物质的量之比为8:4:1,可计算KCl和K2SO4的物质的量,利用m=nM来计算它们的质量.
解答 解:428gNH4Cl的物质的量为:$\frac{428g}{53.5g/mol}$=8mol,
由NH4Cl、K2SO4、KCl三种固体原料的物质的量之比为8:4:1可知,
则KCl的物质的量为1mol,其质量为:1mol×74.5g/mol=74.5g,即a=74.5;
K2SO4的物质的量为4mol,其质量为:4mol×174g/mol=696g,即b=696,
故选C.
点评 本题考查物质的量的计算,为高频考点,题目难度不大,侧重于学生的分析能力和计算能力的考查,明确质量、物质的量的关系即可解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | HCl、HBr、HI、HF的沸点依次升高 | |
| B. | 氨分子中N-H键的极性小于水分子中O-H键的极性 | |
| C. | 乙醇分子间存在氢键,乙醛分子间不存在氢键,故乙醇的沸点高于乙醛 | |
| D. | 由于N-H键强于P-H键,故NH3的沸点高于PH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无法比较 | B. | Q1<Q2 | C. | Q1=Q2 | D. | Q1>Q2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )
用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )| X | Y | Z | |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 碘酒 | 分散系 | 混合物 |
| B | 液氯 | 电解质 | 化合物 |
| C | 硫酸钠 | 盐 | 纯净物 |
| D | NaHSO4 | 酸式盐 | 电解质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
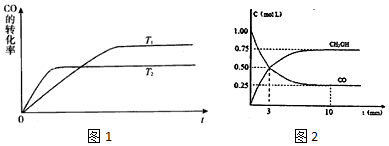
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
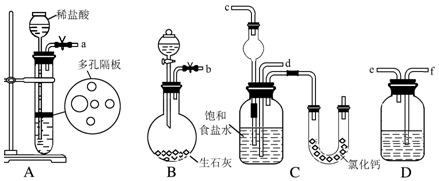
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
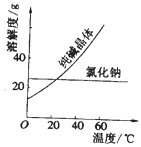
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com